Feliz Año 2.010!!! Líquidos para analizar...
Buenas noches!!! y Feliz Año 2.010!!!
Desde esta "Aula Virtual" les deseo todo lo mejor para este año que recién inicia!!!
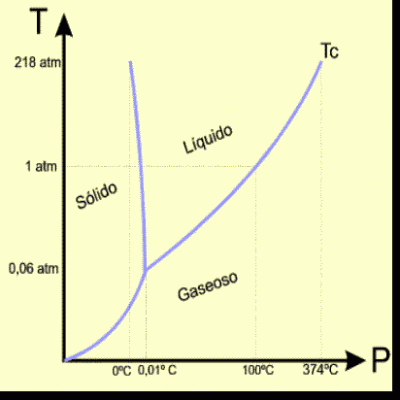
Espero que participen con mayor interés en las actividades virtuales... como la que les planteo hoy: Los líquidos puros presentan un diagrama de fases como el que ilustra esta nota... ¿cómo se interpreta ese gráfico? ¿qué relación puede tener con las actividades que se desarrolla en su carrera?
Saludos!!!
38 comentarios
jesiree diaz 20194534 ng petroqumica 005 -
brian navarro -
raigelys querales C.I:19525349 seccion 005 petroquimica -
- las fases presentes para cada temperatura y composición
- solubilidades a diferentes temperaturas de un componente en otro
- temperatura de solidificación, etc.
Los diagramas de fases se construyen a partir de datos experimentales de Análisis Térmico diferencial (ATD), observación metalográfica y difracción de rayos X.
es importante porq nos ayuda a conocer q son las materias y los estados fisicos
jonathan quiñones C.I:19479058 ing petroquimica seccion 005 -
En ciencia de materiales se utilizan ampliamente los diagramas de fase binarios, mientras que en termodinámica se emplean sobre todo los diagramas de fase de una sustancia pura.
es muy imporantne porqu en un futuro trabajaremos mucho utilizando estos procesos..
norgelis campos C.I:19772161 ing petroquimica 005 -
Los elementos químicos y las sustancias formadas por ellos salvo algunas excepciones, pueden existir en tres estados diferentes: sólido, líquido y gaseoso en dependencia de las condiciones de presión y temperatura en las que se encuentren. El diagrama que representa el tránsito entre estos estados, se conoce como diagrama de fases.
En los ejes están representados los valores de presión y temperatura.
Si el punto de presión y temperatura en que está la sustancia cae en alguna de las áreas señaladas como sólido, liquido o gas, ese será su estado para esas condiciones.
y es muy importante para nuestra carrera ya se relaciona mucho con ella..
Victoria Vasquez -
Ing. Civil 003-D
2 semestre
referente a la grafica se puede deducir que cada compuesto pasa por procesos de cambio de fase o transformaciones, bien sea liquido, solido o gas. teniendo en cuenta que su estado o proceso por el cual se encuentre se debe a la presion y temperatura. Sabiendo que hay un punto donde existen las tres fases simultaneamente.
relacionandolo con la carrera de ing. Civil podria decir que nos ayuda a reconocer los procesos o cambios d fase por los cuales pasan los diferentes estados (solido, liquido, gaseoso).
reina heimar gonzalez II semestre ing petroquimica -
1) por llamarla la primera fase basica es q Pueden adaptarse al espacio fisico en el que se encuentra
2) Se puede encontrar en equilibrio con su estado gaseoso mediante la presión de vapor, entre otras.
como se puede observar en la imagen se presentan los procesos de los liquidos si se llegare a incrementarse la temperatura dara origen o habrá una incrementación de la presion de vapor hasta que se hace similar a la atmosférica pasando del estado liquido al estado gaseoso...y estos distintos procesos de fases los aplicaremos en un futuro en las industrias quimicas ya que se analizaran y se practicaran para crear nuevos productos agregandolos a las diferentes industrias
Martinez Roxana -
roxana martinez -
Carol Andrade -
Seccion I.005 Ing petroquimica
Los elementos químicos y las sustancias formadas por ellos salvo algunas excepciones, pueden existir en tres estados diferentes: sólido, líquido y gaseoso en dependencia de las condiciones de presión y temperatura en las que se encuentren. El diagrama que representa el tránsito entre estos estados, se conoce como DIAGRAMA DE FASES. En su representacion nos ilustra el preceso que alli que realiza como las sustancias (liquidas, solidas, gaseosas) nuestran un procedimiento en cuanto al tipo de estado en que llegaran a estar de pende del punto de presión y temperatura en que está la sustancia cae en alguna de las áreas señaladas de la msima para lograr el estado ya sea de un estado gaseoso a liduidos y solidos y con respecto a nuestra carrera (petroquimica) es fundamental tener este tipo de concepto y entendimiento a la mano ya es requerido porque son los estados y unicos conocidos por la quimica y este proceso se relaciona con la misma.
magdalena torres 20649580 ing civil -
Leandro D. Quiroz G. -
Seccion:I-003D
Se puede interpretar el diagrama que a diferentes temperaturas y precion, los liquidos puros pueden sufrir una trasnformacion o cambio de fase; como lo muestra en el diagrama que de menor a mayor temperatura y precion el gas pasa un solido y por ultimo a un liquido. en el caso de ING. CIVIL seria muy conocer esas etapas y conocer sus propiedades ya que en un futuro trbajaremos con muchos materiales desconosidos.
Leandro Quiroz -
ana gallardo seccion i005 petroquimica -
maria perdomo seccion: I005D ing. petroquimica 2º semestre -
teorileth chavez C.I:21097130 seccion:I005D petroquimica II semestre -
Yulay Acosta -
Cedula:22.728.655
Secciom: I.005 Ing petroquimica
Hola profe buenas Noches.
Segun la graficas,podemos apreciar los cambios o fases que ocurre la materia para llegar a su estado liquido..en la primera parte de la grafica podemos encontrar la materia en estado de gas, luego en la segunda fese pasa la materia a solido y por ultimo culmina siendo un liquido todo esto lo podemos apreciar por los cambios de temperatura de la mas baja hasta ir subiendo y llegar a su mayor temperatura que es cuando la materia llega a asu estado liquido....Los líquidos puros son compuestos que presentan muchas características:
*Pueden adaptarse al espacio fisico en el que se encuentra
*Se puede encontrar en equilibriocon su estado gaseoso mediante la presión de vapor, entre otras.
y con respecto a nuestra carrera es muy importante ya debemos pensar como ing petroquimicos en una manera ampliada para hasi facilitar nuestro trabajo en industrias petroleras e/o...
yessica flores -
19.992.706
Ing.Civil I-003
En este diagrama se puede interpretar el proceso de las fases del agua: en donde se encuentran un estado liquido, solido y gaseaso; en el cual se pueden encontrar un punto critico y un punto triple,dode dichas sustancias varian de acuerdo a la presion y temperatura de la misma.
Con respecto a la relacion con la carrera se puede decir que nos ayuda en el estudio para aprender a reconocer y utilizar las distintas fases y estado a la hora d ponerlo en practica.
geirymar aguirre -
ing. petroquimica
- Es decir que la curva que separa las fases vapor-líquido se detiene en un punto llamado punto crítico. Más allá de este punto, la materia se presenta como un fluido supercrítico que tiene propiedades tanto de los líquidos como de los gases. Modificando la presíón y temperatura en valores alrededor del punto crítico se producen reacciones que pueden tener interés industrial, como por ejemplo las utilizadas para obtener café descafeinado.
Es preciso anotar que, en el diagrama PV del agua, la línea que separa los estados líquido y sólido tiene pendiente negativa, lo cual es algo bastante inusual. Esto quiere decir que aumentando la presíon el hielo se funde, y también que la fase sólida tiene menor densidad que la fase líquida.
paolix oropeza ing civil I-003 -
p=pgz
Donde ¦Ñ es la densidad del l¨ªquido y z es la distancia del punto debajo de la superficie
desde la perpectiva visual segun dicho grafico
Los l¨ªquidos presentan tensi¨®n superficial y capilaridad, generalmente se expanden cuando se incrementa su temperatura y se comprimen cuando se enfr¨ªan. Los objetos inmersos en alg¨²n l¨ªquido son sujetos a un fen¨®meno conocido como flotabilidad.
Las mol¨¦culas en el estado l¨ªquido ocupan posiciones al azar que var¨ªan con el tiempo. Las distancias intermoleculares son constantes dentro de un estrecho margen.
Cuando un l¨ªquido sobrepasa su punto de ebullici¨®n cambia su estado a gaseoso, y cuando alcanza su punto de congelaci¨®n cambia a s¨®lido.
Por medio de la destilaci¨®n fraccionada, los l¨ªquidos pueden separarse de entre s¨ª al evaporarse cada uno al alcanzar sus respectivos puntos de ebullici¨®n. La cohesi¨®n entre las mol¨¦culas de un l¨ªquido no es lo suficientemente fuerte por lo que las mol¨¦culas superficiales se pueden evaporar.
L¨ªquidos, sustancias en un estado de la materia intermedio entre los estados s¨®lido y gaseoso. Las mol¨¦culas de los l¨ªquidos no est¨¢n tan pr¨®ximas como las de los s¨®lidos, pero est¨¢n menos separadas que las de los gases. En algunos l¨ªquidos, las mol¨¦culas tienen una orientaci¨®n preferente, lo que hace que el l¨ªquido presente propiedades anis¨®tropas (propiedades, como el ¨ªndice de refracci¨®n, que var¨ªan seg¨²n la direcci¨®n dentro del material). En condiciones apropiadas de temperatura y presi¨®n, la mayor¨ªa de las sustancias puede existir en estado l¨ªquido. A presi¨®n atmosf¨¦rica, sin embargo, algunos s¨®lidos se subliman al calentarse; es decir, pasan directamente del estado s¨®lido al estado gaseoso (v¨¦ase Evaporaci¨®n). La densidad de los l¨ªquidos suele ser algo menor que la densidad de la misma sustancia en estado s¨®lido. Algunas sustancias, como el agua, son m¨¢s densas en estado l¨ªquido.
jose vidal -
C.I: 22984980
carreta petroquimica
seccion : i 005
se obtienen determinados compuestos que son la base de diversas cadenas productivas que determinan en una amplia gama de productos denominados petroquímicos utilizados en las industrias de fertilizantes, plásticos, alimenticia, farmacéutica, química y textil, entre otras. Las principales cadenas petroquímicas son las del gas natural, las olefinas ligeras (etileno, propileno y butenos) y la de los aromáticos.
A partir del gas natural se produce el gas de síntesis que permite la producción a gran escala de hidrógeno, haciendo posible la producción posterior de amoníaco por su reacción con nitrógeno, y de metanol, materia prima en la producción de metil-terbutil-éter, entre otros compuestos.
Del etileno se producen un gran número de derivados, como las diferentes clases de polietileno, cloruro de vinilo, compuestos clorados, oxidos de etileno, monómeros de estireno entre otros que tienen aplicación en plásticos, recubrimientos, moldes, etc.
Del propileno se producen compuestos como alcohol isopropílico, polipropileno y acrilonitrilo, que tienen gran aplicación en la industria de solventes, pinturas y fibras sintéticas.
Por deshidrogenación de butenos, o como subproducto del proceso de fabricación de etileno se obtiene el 1.3-butadieno que es una materia prima fundamental en la industria de los elastómeros, para la fabricación de llantas, sellos, etc.
Una cadena fundamental en la industria petroquímica se basa en los aromáticos (benceno, tolueno y xilenos). El benceno es la base de produccion de ciclohexano y de la industria del nylon; así como del cumeno para la producción industrial de acetona y fenol. Los xilenos son el inicio de diversas cadenas petroquímicas, principalmente las de las fibras sintéticas.
geirymar aguirre -
ing. petroquimica
- se dice que la curva que separa las fases vapor-líquido se detiene en un punto llamado punto crítico. Más allá de este punto, la materia se presenta como un fluido supercrítico que tiene propiedades tanto de los líquidos como de los gases. Modificando la presíón y temperatura en valores alrededor del punto crítico se producen reacciones que pueden tener interés industrial, como por ejemplo las utilizadas para obtener café descafeinado.
Es preciso anotar que, en el diagrama PV del agua, la línea que separa los estados líquido y sólido tiene pendiente negativa, lo cual es algo bastante inusual. Esto quiere decir que aumentando la presíon el hielo se funde, y también que la fase sólida tiene menor densidad que la fase líquida
jhon quevedo -
la relacion que tiene este diagrama de fases es que el solido es mas importante,ya que nos permitira hacer para las contrucciones.
joseluis figueira ING.Petroquimica seccion:I-005 -
el grafico nos enseña los estados que son el solido,liquido y gaseoso este procedimiento debe tener una cierto presión para que se cumplan todos los procesos de estado.
en mi carrera es muy importante ya que esto esta vinculado con mi carrera
katherine alvarado. seccion i005d Ing-PQ. -
lo cual el grafico representa como primera fase un estado gaseoso, como segundo lugar a un solido y de tal manera llega a una fase culminar como liquido, esto depende de la temperatura.
en cuanto a la relacion q tiene con mi carrera es de suma importancia ya que en un futuro voy a trabajar con cada proceso vinculado a la Ing-PQ
Lilibeth Martinez -
Ing Civil
003
interpretando la grafica se observo que el vapor para el agua liquida y agua solida la linea para el liquido se detiene en el punto critico porque la distincion entre el liquido y gas se desvanece a alta temperatura
la relaciona que puede terner esto en la carrera de ing civil es que el solido tiene mucha relacion porque es necesaria para la contruccion de obras
luz marina -
Ing. civil
003
2 Semetres
con respecto a la interpretacion del grafico podemos decir que el diagrama de fase permite determinar el estado mas estable para
una sustancia a una presion y tenperatura dada. el punto triple de un diagrama de fase da la condicion en la que podemos tener los tres estados en equilibrios.
esto se puede relacionar en nuestra carrera de ing civil cada uno de ellos yiene su importacia pero para nosotro seria mas el solido porque nos ayudaria la construcciones de los material para realizar cualquier obra
maria alejandra urbina I003D Ing. Civil 2 Semestre -
Si el punto de presión y temperatura en que está la sustancia cae en alguna de las áreas señaladas como sólido, liquido o gas, ese será su estado para esas condiciones. Veamos:
Si consideramos que la presión a que está la sustancia es P, entonces para temperaturas menores que T₁ será sólida, para temperaturas entre T₁ y T₂ será líquida y por encima de T₂ gaseosa. Si este punto coincide con alguna se las curvas, coexistirán en equilibrio ambos estados, así si está sobre AB la sustancias será parcialmente sólida y parcialmente gaseosa, si es sobre BD será parcialmente líquida y parcialmente sólida y sobre BC lo mismo entre los estados líquido y gaseoso.
De manera de relacionar este diagrama con la carrera q estamos cursando, se puede decir, que son la pasos q podemos utilizar. En caso de la Ing, Civil se puede decir, que es la forma de como podemos indetentificar las fases ( solido, liquido, gaseoso ).
jose rosales 2do semestre de petroquimica seccion i005 -
jorman caraballo petroquimica I005 2do semetre -
joel pereira Petroquimica I005 2do semestre -
joel pereira Petroquimica I005 2do semestre -
jose paredes petroquimica i005 2do semestre -
JESUS VALLEJO c.i 2226869 ing. petro quimica semestre 2 -
pedro lopez ci:22518611 ing petoquimica i005 2do semestre -
JHON MONTOYA SECCION I-005 DE 2 DO SEMESTRE ING PETROQUIMICA -
y en cuanto a las actividades que se dersarrollan en nuestra carrera son los procesos que mas se presentan en las industrias ya sea para la creacion de un producto u obtension de una materia prima en la s industrias de polimeros e industrias de fertilizantes como en la refinacion del petroleo en la elaborcion de medicamentos en todos lon ambitos empresariales se presentan los liquidos gases y solidos ya no sea directamente en el producto pero si en algun momento de su elaboracion.
Luis Arvelo CI. 22.414.117 Ing. Petroquimica 2do semestre -
1) Pueden adaptarse al espacio fisico en el que se encuentra
2) Se puede encontrar en equilibriocon su estado gaseoso mediante la presión de vapor, entre otras.
como se observa en el dibujo se denotan los procesos de los liquidos puros si se incrementa la temperatura habrá una incrementación de la presion de vapor hasta que se hace similar a la atmosférica pasando de liquido a gaseoso...y estos distintos porcesos de fases los aplicaremos en un futuro en las industrias quimicas ya que se analizaran y se practicaran para crear nuevos productos agregandolos a la industria comercial
Nataly Buinitzky CI.21.327.393 Ing. Petroquímica 2do semestre -
segun las preguntas dadas se puede interpretar el grafico como los procesos o las fases por la que pasa un líquido de acuerdo a la ilustracion se muestra que este en primer lugar es un gas luego en la 2da fase pasa a ser un solido y por último culmina siendo un líquido todo este proceso puede realizarse a travez de altas temperatura claro es que cada una de las fases empieza con una temperatura baja para luego ir aumentando llegando hasta la ultima fase que seria liquido...y respondiendo la 2da pregunta realizada se podria decir que debido a nuestra carrera Ing Petroqímica debemos aprender y comprender cada uno de los pasos para extraer y convertir los gases, líquidos y sólidos para obtener productos que nos puedan servir en la vida cotidiana y analizar cada uno de los procesos de las industrias petroleras y quimicas..