Estructura Electrónica y Propiedades Periódicas
Buenos días!!!
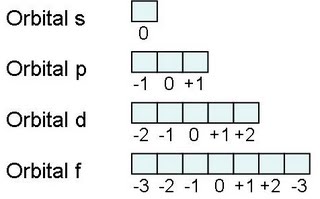
Hemos estado conversado sobre la estructura electrónica de los elementos, y por ello les recomiendo que observen la página http://es.wikipedia.org/wiki/Configuraci%C3%B3n_electr%C3%B3nica, en donde se presenta todo lo conversado, y algo más, especialmente lo relacionado a las excepciones en el desarrollo de la distribución electrónica, que como sabemos es la distribución de los electrones en los subniveles y orbitales de un átomo. La configuración electrónica de los elementos se rige según el “método de la lluvia”, también llamado “diagrama de Moeller”, el cual debe respetar ciertas normas o “reglas” que se mencionan en esta página de Wikipedia. Igualmente, pueden ver las páginas http://www.netcom.es/pilar_mu/atomos.htm y http://iiquimica.blogspot.com/2008/04/nmeros-cunticos-y-configuracin.html, donde se expresan estos conceptos de manera directa.
Con respecto a las propiedades periódicas, pueden obtener un documento PDF de la página http://webdelprofesor.ula.ve/ingenieria/claudiag/DocuIPQ/Tabla%20periodica%20propiedades.pdf, donde se comentan las propiedades periódicas de los elementos, y en Wikipedia (http://es.wikipedia.org/wiki/Categor%C3%ADa:Propiedades_peri%C3%B3dicas) hay un listado de propiedades periódicas que pueden observar con toda la calma, ya que ese será el tema de análisis del próximo martes.
Para esta semana, les propongo seleccionen un elemento químico (diferente para cada estudiante, por favor!!!), y presenten sus propiedades químicas más importantes, relacionándolas con su distribución electrónica.
Saludos!!!
38 comentarios
Brian Navarro -
Seccion:I.005 ing petroquimica
El mercurio o azogue o ☿ es un elemento químico de número atómico 80. Su nombre y abreviatura (Hg) procede de hidrargirio, término hoy ya en desuso, que a su vez procede del latín hidrargirium y de hydrargyrus, que a su vez proviene del griego hydrargyros (hydros = agua y argyros = plata).
Es un metal pesado plateado que a temperatura ambiente es un líquido inodoro. Es mal conductor del calor comparado con otros metales, aunque no es mal conductor de la electricidad. Se alea fácilmente con muchos otros metales como el oro o la plata produciendo amalgamas, salvo con el hierro. Es insoluble en agua y soluble en ácido nítrico. Cuando aumenta su temperatura produce vapores tóxicos y corrosivos, más pesados que el aire. Es dañino por inhalación, ingestión y contacto. Producto muy irritante para la piel, ojos y vías respiratorias. Es incompatible con el ácido nítrico concentrado, el acetileno, el amoníaco, el cloro y los metales.
El mercurio es un elemento "anómalo" en varias propiedades. Es un metal noble, ya que su potencial redox Hg2+/Hg es positivo (+0,85 V), frente al negativo de Cd (-0,40 V), su vecino inmediato de grupo. Es un metal singular con algo de parecido al cadmio, pero es más semejante al oro y al talio. Es el único metal de transición líquido con una densidad tan elevada, 13,53 g/cm3; una columna de 76 cm define una atmósfera, mientras que con agua necesitamos 10m de altura. Su estado líquido en condiciones estándar nos indica que su enlace metálico es débil y se justifica por la poca participación de los electrones 6s2 a la delocalización electrónica en el sistema metálico (efectos relativistas). Tiene la primera energía de ionización más alta de todos los metales por la misma razón anterior. Además el Hg2+ tiene muy baja entalpía de hidratación comparada con la del Zn2+ y Cd2+, con preferencia por la coordinación dos en los complejos de Hg (II), como el Au (I) isoelectrónico. Esto trae como consecuencia que los potenciales redox de aquellos sean negativos y el del mercurio sea noble (positivo). La poca reactividad del mercurio en procesos oxidativos hay que razonarla por los efectos relativistas sobre los electrones 6s2 muy contraídos hacia el núcleo y por la fortaleza de su estructura electrónica de pseudogas noble. También es el único elemento del grupo que presenta el estado +I, en forma de especie dinuclear Hg22+, aunque la tendencia general a estabilizar los estados de oxidación bajos sea la contraria en los grupos de transición: formación de compuestos de Hg (I) con pares clusters Hg-Hg. Esta rica covalencia también la podemos ver en compuestos de Hg (II), donde tenemos muchos compuestos de Hg (II) que son volátiles como el HgCl2, sólido molecular con entidades Cl-Hg-Cl en sólido, vapor e incluso en disolución acuosa. Podemos destacar también la resistencia de amidas, imidas y organometálicos de mercurio a la hidrólisis y al oxígeno del ambiente, lo que nos indica gran fortaleza Hg-C. También el S y el P son átomos dadores adecuados: ligandos blandos efectivos para ácidos blandos como el Hg en estados de oxidación cero, I y II.
El mercurio en su estado más conocido es bivalente, esto es, se asocia con sólo dos átomos, sin embargo en el 2007 se ha descubierto que a bajísimas temperaturas, del orden de -260 °C (esto es la temperatura media del espacio), existe en estado tetravalente pudiendo asociarse con cuatro átomos de flúor y obteniendo de tal modo un grado de oxidación adicional, a esta forma se la denomina tetrafluoruro de mercurio (HgF4); la estructura es plano cuadrada, la de mayor estabilidad para un d8. Este comportamiento es de esperar, ya que el mercurio tiene mayor expansión relativista de sus orbitales 5d en relación a sus homólogos del grupo 12, con lo que frente al fluor, el elemento más oxidante de la tabla periódica, puede en condiciones extremas generar enlaces covalentes. La posibilidad de sintetizar este fluoruro de mercurio, HgF4,fue predicha teóricamente en el 1994 de acuerdo a modelos antes indicados. Por la misma razón podemos considerar la posibilidad del estado de oxidación III para este metal, y efectivamente se ha aislado una especie compleja, en un medio especial y por oxidación electroquímica, donde tenemos el catión complejo,[Hg cyclam]3+; el cyclam es un ligando quelato que estabiliza al mercurio en este estado de oxidación raro (1,4,8,11-Tetraazaciclotetradecane= cyclam). Con todo esto, debemos concluir que el mercurio debe ser rescatado y ser incluido como metal de transición, ya que genera especies en donde participan sus orbitales d internos.
Yulay Acosta -
Seccion: I.005 petroquimica
Elemento Plata:
Elemento químico de número atómico 47 y símbolo Ag (de su denominación latina argentum). Es un metal precioso de color metálico claro que en condiciones normales es sólido. Es uno de los mejores conductores del calor y de la electricidad. Se encuentra raramente en la naturaleza, lo que le hace ser un metal caro. Es muy dúctil y maleable por lo que es especialmente apreciado en joyería. Características principales
La plata es un metal de acuñar muy dúctil y maleable, algo más duro que el oro, que presenta un brillo blanco metálico susceptible de pulimento que se mantiene en agua y aire si bien su superficie se empaña en presencia de ozono, sulfuro de hidrógeno o aire con azufre. Su maleabilidad y ductilidad sólo superadas por el oro son tales que es posible obtener láminas de 0,00025 mm y con 1g de metal fabricar un hilo de 180 metros de longitud.
Tiene la más alta conductividad eléctrica de todos los metales, incluso superior a la del cobre el conductor por excelencia pero su mayor precio ha impedido que se utilice de forma masiva en aplicaciones eléctricas.
La plata pura también presenta la mayor conductividad térmica, el color más blanco y el mayor índice de reflexión (aunque refleja mal la radiación ultravioleta) de todos los metales. Algunas sales de plata son fotosensibles (se descomponen por acción de la luz) y se han empleado en fotografía.
Se disuelve en ácidos oxidantes y puede presentar los estados de oxidación +1, +2 y +3, siendo el más común el estado de oxidación +1.
El uso principal de la plata es como metal precioso, y sus sales, especialmente el nitrato de plata se emplean en la industria fotográfica, con mucho la mayor consumidora de este metal. Otros usos son:
Electricidad y electrónica por su elevada conductividad incluso empañado, por ejemplo en los contactos de circuitos integrados y teclados de ordenador.
Espejos de gran reflectividad de la luz visible (los comunes que se fabrican con aluminio).
La plata se ha empleado para fabricar monedas desde 700 adC, inicialmente con electrum, aleación natural de oro y plata, y más tarde de plata pura.
En joyería y platería para fabricar gran variedad de artículos y con menor grado de pureza en artículos de bisutería.
En aleaciones para piezas dentales.
Catalizador en reacciones de oxidación, por ejemplo, en la producción de formaldehído a partir de metanol y aire.
Aleaciones para soldadura, contactos eléctricos y baterías eléctricas plata-cinc y plata-cadmio de alta capacidad.
El folclore popular atribuye a la plata propiedades mágicas para derrotar a criaturas supernaturales como vampiros y hombres lobo.
La plata natural se compone de dos isótopos estables Ag-107 y Ag-109, siendo el primero ligeramente más abundante (51,839%) que el segundo. Se han caracterizado veintiocho radioisótopos de los cuales los más estables son la Ag-105, Ag-11 y Ag-112, con vidas medias de 41,29 días, 7,45 días y 3,13 horas respectivamente. Los demás isótopos tienen periodos de semidesintegración más cortos que una hora, y la mayoría menores que tres minutos. Se han identificado numerosos estados metaestables entre los cuales los mas estables son Agm-128 (418 años), Agm-110 (249,79 días) y Agm-107 (8,28 días).
Los isótopos de la plata tienen pesos atómicos que varían entre las 93,943 uma de la Ag-94 y las 123,929 uma de la Ag-124. El modo de desintegración principal de los isótopos más ligeros que el estable más abundante es la captura electrónica resultando isótopos de paladio, mientras que los isótopos más pesados que el estable más abundante se desintegran sobre todo mediante emisión beta dando lugar a isótopos de cadmio.
El isótopo Pd-107 se desintegra mediante emisión beta produciendo Ag-107 y con un periodo de semidesintegración de 6,5 millones de años. Los meteoritos férreos son los únicos objetos conocidos con una razón Pd/Ag suficientemente alta para producir variaciones medibles en la abundancia natural del isótopo Ag-107. La Ag-107 radiogenética se descubrió en el meteorito de Santa Clara (California en 1978 (ver Isótopos del paladio).
maria gabriela jimenez -
ING. PETROQUIMICA
SODIO:es un elemento químico de símbolo Na (del latín, natrium) y número atómico 11, fue descubierto por Sir Humphry Davy. Es un metal alcalino blando, untuoso, de color plateado, muy abundante en la naturaleza, encontrándose en la sal marina y el mineral halita. Es muy reactivo, arde con llama amarilla, se oxida en presencia de oxigeno y reacciona violentamente con el agua.
El sodio está presente en grandes cantidades en el océano en forma iónica. También es un componente de muchos minerales y un elemento esencial para la vida.
CARACTERISTICAS:
Al igual que otros metales alcalinos el sodio es un metal blando, ligero y de color plateado que no se encuentra libre en la naturaleza. El sodio flota en el agua descomponiéndola, desprendiendo hidrógeno y formando un hidróxido. En las condiciones apropiadas reacciona espontáneamente en el agua. Normalmente no arde en contacto con el aire por debajo de 40 °C. USOS DEL SODIO: El sodio metálico se emplea en síntesis orgánica como agente reductor. Es además componente del cloruro de sodio necesario para la vida. Otros usos son:
En aleaciones antifricción (oro).
En la fabricación de desodorantes (en combinación con ácidos grasos).
En la purificación de metales fundidos.
La aleación Na K, es un material empleado para la transferencia de calor además de desecante para disolventes orgánicos y como reductor. A temperatura ambiente es líquida. El sodio también se emplea como refrigerante.
Aleado con plomo se emplea en la fabricación de aditivos detonantes para las gasolinas.
Se emplea también en la fabricación de células fotoeléctricas.
Iluminación mediante lámparas de vapor de sodio.
Los óxidos NaO2 generados por combustión controlada con oxígeno se utilizan para intercambiar el dióxido de carbono por oxígeno y regenerar así el aire en espacios cerrados
COMPUESTOS
Los compuestos de sodio de mayor importancia industrial son:
Sal común (NaCl).
Carbonato de sodio (Na2CO3).
Bicarbonato de sodio (NaHCO3).
DISTRIBUCION DE ELECTRONES
Z=11
1S2 2S2 2P5 3S2.
yoel sequera seccion I003 ing civil -
Cromo
Número atómico
24
Valencia
2,3,4,5,6
Estado de oxidación
+3
Electronegatividad
1,6
Radio covalente (Å)
1,27
Radio iónico (Å)
0,69
Radio atómico (Å)
1,27
Configuración electrónica
[Ar]3d54s1
Primer potencial de ionización (eV)
6,80
Masa atómica (g/mol)
51,996
Densidad (g/ml)
7,19
Punto de ebullición (ºC)
2665
Punto de fusión (ºC)
1875
Descubridor
Vaughlin en 1797
El cromo es un elemento químico de número atómico 24 que se encuentra en el grupo 6 de la tabla periódica de los elementos. Su símbolo es Cr. Es un metal que se emplea especialmente en metalurgia.
El cromo es un metal de transición duro, frágil, gris acerado y brillante. Es muy resistente frente a la corrosión.
Su estado de oxidación más alto es el +6, aunque estos compuestos son muy oxidantes. Los estados de oxidación +4 y +5 son poco frecuentes, mientras que los estados más estables son +2 y +3. También es posible obtener compuestos en los que el cromo presente estados de oxidación más bajos, pero son bastante raros.
[editar] Compuestos
El dicromato de potasio, K2Cr2O7, es un oxidante enérgico y se utiliza para limpiar material de vidrio de laboratorio de cualquier resto orgánico que pueda contener.
El "verde de cromo" (es el óxido de cromo (III), Cr2O3) es un pigmento que se emplea, por ejemplo, en pinturas esmaltadas y en la coloración de vidrios. El "amarillo de cromo" (es un cromato de plomo, PbCrO4) también se utiliza como pigmento.
No se encuentran en la naturaleza ni el ácido crómico ni el dicrómico, pero sus aniones se encuentran en una amplia variedad de compuestos. El trióxido de cromo, CrO3, el que sería el anhídrido del ácido crómico, se vende industrialmente como "ácido crómico". Empleado como uno de los componentes del proceso de los baños de cromado
mayra roa -
005
21628070
Propiedades químicas del Galio - Efectos del Galio sobre la salud - Efectos ambientales del Galio
Nombre
Galio
Número atómico
31
Valencia
3
Estado de oxidación
+3
Electronegatividad
1,6
Radio covalente (Å)
1,26
Radio iónico (Å)
0,62
Radio atómico (Å)
1,41
Configuración electrónica
[Ar]3d104s24p1
Primer potencial de ionización (eV)
6,02
Masa atómica (g/mol)
69,72
Densidad (g/ml)
5,91
Punto de ebullición (ºC)
2237
Punto de fusión (ºC)
29,8
Galio
Elemento químico, símbolo Ga, número atómico 31 y peso atómico 69.72. lo descubrió Lecoq de Boisbaudran en Francia en 1875. Tiene un gran intervalo de temperatura en el estado líquido, y se ha recomendado su uso en termómetros de alta temperatura y manómetros. En aleación con plata y estañó, el galio suple en forma adecuada la amalgama en curaciones dentales; también sirve para soldar materiales no metálicos, incluyendo gemas o amtales. El arseniuro de galio puede utilizarse en sistemas para transformar movimiento mecánico en impulsos eléctricos. Los artículos sintéticos superconductores pueden prepararse por la fabricación de matrices porosas de vanadio o tántalo impregnados con hidruro de galio. El galio ha dado excelentes resultados como semiconductor para uso en rectificadores, transistores, fotoconductores, fuentes de luz, diodos láser o máser y aparatos de refrigeración.
El galio sólido parece gris azulado cuando se expone a la atmósfera. El galio líquido es blanco plateado, con una superficie reflejante brillante. Su punto de congelación es más bajo que el de cualquier metal con excepción del mercurio (-39ºC o -38ºF) y el cesio (28.5ºC u 83.3ºF).
El galio es semejante químicamente al aluminio. Es anfótero, pero poco más ácido que el aluminio. La valencia normal del galio es 3+ y forma hidróxidos, óxidos y sales. El galio funde al contacto con el aire cuando se calienta a 500ºC (930ºF). Reacciona vigorosamente con agua hirviendo, pero ligeramente con agua a temperatura ambiente. Las sales de galio son incoloras; se preparan de manera directa a partir del metal, dado que la purificación de éste es más simple que la de sus sales.
El galio forma aleaciones eutécticas de bajo punto de fusión con varios metales, y compuestos intermetálicos con muchos otros. Todo el aluminio contiene cantidades pequeñas de galio, como impureza inofensiva, pero la penetración intergranular de grandes cantidades a 30ºC causa fallas catastróficas.
dayana oliveros CI: 20663015 II Semestre Petroquimica I005 -
En sus compuestos presenta variados estados de oxidación, siendo los más comunes +2, +3, +4 y +5.
VANADIO (V) 23
Peso atómico 50,9415 g/mol
Estados oxidación 5, 4, 3, 2
Punto de fusión 2136 K
Punto de ebullición 3650 K
Densidad 6,11 g/cm³
Configuración electrónica [Ar] 3d3 4s2
Propiedades ácido/base Anfótero
Estructura cristal Cúbico, centrado en cuerpo
Electronegatividad 1,63
Calor de vaporización 446,7 kJ/mol
Calor de fusión 22,8 kJ/mol
Conductividad eléctrica 4,0 106 W-¹m-¹
Conductividad térmica 30,7 Wm-¹K-¹ (a 300 K)
Calor específico 0,489 Jg-¹K-¹ (a 300 K)
Primer potencial ionización 6,74
Volumen atómico 8,35 cm³/mol
Radio atómico 1,34 Å
Radio covalente 1,22 Å
Sintético No
dayana oliveros CI: 20663015 II Semestre Petroquimica I005 -
El titanio es un elemento químico, de símbolo Ti y número atómico 22. Se trata de un metal de transición de color gris plata. Comparado con el acero, metal con el que compite en aplicaciones técnicas, es mucho más ligero (4,5/7,8). Tiene alta resistencia a la corrosión y gran resistencia mecánica, pero es mucho más costoso que el acero, lo cual limita su uso industrial.
Es un metal abundante en la naturaleza; se considera que es el cuarto metal estructural más abundante en la superficie terrestre y el noveno en la gama de metales industriales. No se encuentra en estado puro sino en forma de óxidos, en la escoria de ciertos minerales de hierro y en las cenizas de animales y plantas. Su utilización se ha generalizado con el desarrollo de la tecnología aeroespacial, donde es capaz de soportar las condiciones extremas de frío y calor que se dan en el espacio y en la industria química, por ser resistente al ataque de muchos ácidos; asimismo, este metal tiene propiedades biocompatibles, dado que los tejidos del organismo toleran su presencia, por lo que es factible la fabricacion de muchas prótesis e implantes de este metal.
Posee propiedades mecánicas parecidas al acero, tanto puro como en las aleaciones que forma, por tanto compite con el acero en muchas aplicaciones técnicas, especialmente con el acero inoxidable.
El titanio fue declarado material estratégico por parte de Estados Unidos durante muchos años. Puede formar aleaciones con otros elementos, tales como hierro, aluminio, vanadio, molibdeno y otros, para producir componentes muy resistentes que son utilizados por la industria aeroespacial, aeronáutica, militar, petroquímica, agroindustrial, automovilística y médica.
TITANIO (Ti)22
Peso atómico 47,867 g/mol
Estados oxidación 4, 3
Punto de fusión 1935 K
Punto de ebullición 3560 K
Densidad 4,54 g/cm³
Configuración electrónica [Ar] 3d2 4s2
Propiedades ácido/base Anfótero
Estructura cristal Hexagonal
Electronegatividad 1,54
Calor de vaporización 425,2 kJ/mol
Calor de fusión 18,6 kJ/mol
Conductividad eléctrica 2,6 106 W-¹m-¹
Conductividad térmica 21,9 Wm-¹K-¹ (a 300 K)
Calor específico 0,523 Jg-¹K-¹ (a 300 K)
Primer potencial ionización 6,82
Volumen atómico 10,60 cm³/mol
Radio atómico 1,45 Å
Radio covalente 1,32 Å
Sintético No
rosimar oropeza C.I: 21097560 seccion: I005D petroquimica II semestre -
nº atomico: 75
simbolo: Re´
El renio es un elemento químico de número atómico 75 situado en el grupo 7 de la tabla periódica de los elementos que tiene como símbolo Re.
Es un metal de transición blanco plateado, pesado, que se encuentra raramente en la naturaleza. El renio se obtiene como subproducto del tratamiento de minerales de molibdeno. Ha sido el último elemento que se ha podido encontrar en la naturaleza. Se emplea principalmente formando parte en catalizadores.
jorman caraballo 21.021.415 II semetre ing. petroquimica -
Zirconio
Número atómico
40
Valencia
2,3,4
Estado de oxidación
+4
Electronegatividad
1,4
Radio covalente (Å)
1,48
Radio iónico (Å)
0,80
Radio atómico (Å)
1,60
Configuración electrónica
[Kr]4d25s2
Primer potencial
de ionización (eV)
6,98
Masa atómica (g/mol)
91,22
Densidad (g/ml)
6,49
Punto de ebullición (ºC)
3580
Punto de fusión (ºC)
1852
Descubridor
Martin Klaproth en 1789
Zirconio
Elemento químico de símbolo, Zr, número atómico 40 y peso atómico 91.22. Se encuentran en la naturaleza los siguientes isótopos: 90, 91, 94 y 96. El zirconio es uno de los elementos más abundantes y está ampliamente distribuido en la corteza terrestre. Es muy reactivo químicamente y sólo se halla combinado. En la mayor parte de las reacciones se enlaza con oxígeno en preferencia sobre otros elementos, encontrándose en la corteza terrestre sólo como el óxido ZrO2, baddeleyita, o como parte de los complejos de óxido, como el zircón, la elpidita y la eudialita. Desde el punto de vista comercial, el zircón es su mineral más importante. El zirconio y hafnio son prácticamente indistinguibles en sus propiedades químicas, y sólo se les encuentra juntos.
El mayor empleo del zirconio corresponde a sus compuestos para la industria cerámica: refractarios, vidriados, barnizados, moldes fundidos y arenas abrasivas, componentes de cerámica eléctrica. La incorporación del óxido de zirconio al vidrio incrementa significativamente su resistencia a los álcalis. El zirconio metálico se utiliza casi exclusivamente para el revestimiento de los elementos combustibles de uranio en las plantas nucleares. Otra aplicación significativa es la de los flash fotográficos.
dayana oliveros CI: 20663015 II Semestre Petroquimica I005 -
Símbolo Ni, número atómico 28, metal duro, blanco plateado, dúctil y maleable. La masa atómica del níquel presente en la naturaleza es 58.71.
El níquel tiene cinco isótopos naturales con masas atómicas de 58, 60, 61, 62, 64. También se han identificado siete isótopos radiactivos, con números de masa de 56, 57, 59, 63, 65, 66 y 67.
La mayor parte del níquel comercial se emplea en el acero inoxidable y otras aleaciones resistentes a la corrosión. También es importante en monedas como sustituto de la plata. El níquel finamente dividido se emplea como catalizador de hidrogenación.
El níquel es un elemento bastante abundante, constituye cerca de 0.008% de la corteza terrestre y 0.01% de las rocas ígneas. En algunos tipos de meteoritos hay cantidades apreciables de níquel, y se piensa que existen grandes cantidades en el núcleo terrestre. Dos minerales importantes son los sulfuros de hierro y níquel, pentlandita y pirrotita (Ni, Fe)xSy; el mineral garnierita, (Ni, Mg)SiO3.nH2O, también es importante en el comercio. El níquel se presenta en pequeñas cantidades en plantas y animales. Está presente en pequeñas cantidades en el agua de mar, el petróleo y en la mayor parte del carbón.
El níquel metálico es fuerte y duro (3.8 en la escala de Mohs), Cuando está finamente dividido, es de color negro. La densidad del níquel es 8.90 veces la del agua a 20ºC (68ºF); se funde a 1455ºC (2651ºF) y hierve a 2840ºC (5144ºF); es sólo moderadamente reactivo. Resiste la corrosión alcalina y no se inflama en trozos grandes, pero los alambres muy finos pueden incendiarse. Está por encima del hidrógeno en la serie electroquímica; se disuelve con lentitud en ácidos diluidos liberando hidrógeno. En forma metálica es un agente reductor fuerte.
El níquel es dipositivo en sus compuestos, pero también puede existir en los estados de oxidación 0, 1+, 3+, 4+. Además de los compuestos simples o sales, el níquel forma una variedad de compuestos de coordinación o complejos. La mayor parte de los compuestos de níquel son verdes o azules a causa de la hidratación o de la unión de otros ligandos al metal. El ion níquel presente en soluciones acuosas de compuestos simples es a su vez un complejo, el [Ni(H2O)6]2+.
Efectos del Níquel sobre la salud
El níquel es un elemento que ocurre en el ambiente sólo en muy pequeños niveles. Los humanos usan el níquel para muchas aplicaciones diferentes. La aplicación más común del níquel es el uso como ingrediente del acero y otros productos metálicos. Este puede ser encontrado en productos metálicos comunes como es la joyería.
Los alimentos naturalmente contienen pequeñas cantidades de níquel. El chocolate y las grasas son conocidos por contener altas cantidades. El níquel es tomado y este aumentará cuando la gente come grandes cantidades de vegetales procedentes de suelos contaminados. Es conocido que las plantas acumulan níquel y como resultado la toma de níquel de los vegetales será eminente. Los fumadores tiene un alto grado de exposición al níquel a través de sus pulmones. Finalmente, el níquel puede ser encontrado en detergentes. Los humanos pueden ser expuestos al níquel al respirar el aire, beber agua, comer comida o fumar cigarrillos. El contacto de la piel con suelo contaminado por níquel o agua puede también resultar en la exposición al níquel. En pequeñas cantidades el níquel es esencial, pero cuando es tomado en muy altas cantidades este puede ser peligroso par la salud humana.
NIQUEL (Ni) 28
Peso atómico 58,6934 g/mol
Estados oxidación 2, 3
Punto de fusión 1726 K
Punto de ebullición 3005 K
Densidad 8,90 g/cm³
Configuración electrónica [Ar] 3d8 4s2
Propiedades ácido/base Básico
Estructura cristal Cúbico, centrado en cara
Electronegatividad 1,91
Calor de vaporización 377,5 kJ/mol
Calor de fusión 17,2 kJ/mol
Conductividad eléctrica 14,6 106 W-¹m-¹
Conductividad térmica 90,7 Wm-¹K-¹ (a 300 K)
Calor específico 0,444 Jg-¹K-¹ (a 300 K)
Primer potencial ionización 7,635
Volumen atómico 6,60 cm³/mol
Radio atómico 1,24 Å
Radio covalente 1,15 Å
Sintético No
ana julia da silva CI: 20760108 II semestre petroquimica I005 -
El plomo es un metal pesado de densidad relativa o gravedad específica 11,4 a 16 °C, de color azuloso, que se empaña para adquirir un color gris mate. Es flexible, inelástico y se funde con facilidad. Su fusión se produce a 327,4 °C y hierve a 1725 °C. Las valencias químicas normales son 2 y 4. Es relativamente resistente al ataque de ácido sulfúrico y ácido clorhídrico, aunque se disuelve con lentitud en ácido nítrico y ante la presencia de bases nitrogenadas. El plomo es anfótero, ya que forma sales de plomo de los ácidos, así como sales metálicas del ácido plúmbico. Tiene la capacidad de formar muchas sales, óxidos y compuestos organometálicos. Los cuatro isótopos naturales son, por orden decreciente de abundancia, 208, 206, 207 y 204. Se cristaliza en el sistema cúbico en forma de cara centrada invertida.
PLOMO (Pb)
Peso atómico 207,2 g/mol
Estados oxidación 2, 4
Punto de fusión 600,65 K
Punto de ebullición 2023 K
Densidad 11,35 g/cm³
Configuración electrónica [Xe] 4f 14 5d10 6s2 p2
Propiedades ácido/base Anfótero
Estructura cristal Cúbico, centrado en cara
Electronegatividad 2,33
Calor de vaporización 177,9 kJ/mol
Calor de fusión 4,77 kJ/mol
Conductividad eléctrica 4,8 106 W-¹m-¹
Conductividad térmica 35,3 Wm-¹K-¹ (a 300 K)
Calor específico 0,129 Jg-¹K-¹ (a 300 K)
Primer potencial ionización 7,416
Volumen atómico 18,30 cm³/mol
Radio atómico 1,75 Å
Radio covalente 1,47 Å
Sintético No
JHON MONTOYA SECCION I-005 2 DO SEMESTRE ING. PETROQUIMICA -
Fr.........El francio es menos estable que cualquier otro elemento más ligero que el nobelio (elemento 102);su isótopo más estable, el 223Fr, posee un período de semidesintegración menor de 22 minutos. El astato, que es el siguiente elemento menos estable, tiene período de semidesintegración máximo de 8,5 horas. Todos los isótopos del francio se desintegran generando astato, radio y radón.
El francio es un metal alcalino cuyas propiedades químicas son semejantes a las del cesio. Puesto que es un elemento muy pesado con un solo electrón de valencia, posee el mayor peso equivalente de todos los elementos químicos. El francio tiene la más baja electronegatividad de todos los elementos conocidos, con un valor de 0,7 en la escala de Pauling. Le sigue el cesio con un valor de 0,79. El francio líquido, en el supuesto de poder ser obtenido, tendría una tensión superficial de 0,05092 J·m2 en el punto de fusión.
El francio coprecipita junto con muchas sales de cesio, como el perclorato de cesio, formando pequeñas cantidades de perclorato de francio. Esta coprecipitación puede emplearse para aislar el francio, adaptando el método de precipitación del radiocesio de Glendenin y Nelson. También coprecipita con otras sales de cesio como el yodato, el picrato, el tartrato (también con el tartrato de rubidio), el cloroplatinato y el silicowolframato. Otras coprecipitaciones se producen con el ácido silicowolfrámico y con el ácido perclórico, sin necesidad de que otro metal alcalino esté presente como portador, lo que posibilita otros métodos de separación para el francio. Casi todas las sales de francio son solubles en agua.
Francio - Fr
Propiedades químicas del Francio - Efectos del Francio sobre la salud - Efectos ambientales del Francio
Nombre
Francio
Número atómico
87
Valencia
1
Estado de oxidación +1
Electronegatividad
0,8
Radio covalente (Å)
-
Radio iónico (Å)
1,76
Radio atómico (Å)
-
Configuración electrónica
[Rn]7s1
Primer potencial de ionización (eV)
-
Masa atómica (g/mol)
223
Densidad (g/ml)
-
Punto de ebullición (ºC)
-
Punto de fusión (ºC)
27
Descubridor
Marguerite Derey en 1939
Francio
Elemento químico, símbolo Fr, número atómico 87, metal alcalino colocado abajo del cesio en el grupo Ia de la tabla periódica. Se distingue por su inestabilidad nuclear, ya que existe sólo en formas radiactivas de vida corta; el más estable tiene una vida media de 21 minutos. El principal isótopo del francio es el actinio-K, isótopo de masa 223, el cual proviene del decaimiento del actinio radiactivo, de las propiedades conocidas, es muy probable que ninguna forma de vida larga del elemento 87 se encuentre en la naturaleza o sintetizada de manera artificial.
Las propiedades químicas del francio pueden estudiarse sólo a la escala de trazas. El elemento muestra todas las propiedades esperadas de los elementos alcalinos más pesados. Con pocas excepciones, todas las sales del francio son solubles en agua.
Efectos del Francio sobre la salud
Al ser tan inestable, cualquier cantidad formada se descompondrá en otros elementos tan rápidamente que no hay motivo para estudiar sus efectos en la salud humana.
Efectos ambientales del Francio
Debido a su vida media tan extremadamente corta, no existe razón para considerar los efectos del francio en el medio ambiente.
(1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s1)
JHON QUEVEDO -
La plata es un elemento químico de número atómico 47 situado en el grupo 1b de la tabla periódica de los elementos. Su símbolo es Ag (procede del latín: argentum). Es un metal de transición blanco, brillante, blando, dúctil, maleable.
Se encuentra en la naturaleza formando parte de distintos minerales (generalmente en forma de sulfuro) o como plata libre. Es muy escasa en la naturaleza, de la que representa una parte en 10 millones de corteza terrestre. La mayor parte de su producción se obtiene como subproducto del tratamiento de las minas de cobre, cinc, plomo y oro. La metalurgia a partir de sus minerales se realiza fundamentalmente por la cianuración:
Ag2S + 4 KCN → K2S + 2 KAg(CN)2
Propiedades generales
La plata es un metal de acuñar muy dúctil y maleable, algo más duro que el oro, la plata presenta un brillo blanco metálico susceptible al pulimento. Se mantiene en agua y aire, si bien su superficie se empaña en presencia de ozono, sulfuro de hidrógeno o aire con azufre. Su maleabilidad y ductilidad sólo superadas por el oro son tales, que es posible obtener láminas de 0,00025 mm[cita requerida] y con 1 g de metal fabricar un hilo de 180 metros de longitud.
Tiene una de las más altas conductividades eléctricas de todos los metales, incluso superior a la del cobre el conductor por excelencia pero su mayor precio ha impedido que se utilice de forma masiva en aplicaciones eléctricas. La plata pura también presenta la mayor conductividad térmica, el color más blanco y el mayor índice de reflexión (aunque refleja mal la radiación ultravioleta) de todos los metales. Algunas sales de plata son fotosensibles (se descomponen por acción de la luz) y se han empleado en fotografía.
Se disuelve en ácidos oxidantes y puede presentar los estados de oxidación +1, +2 y +3, siendo el más común el estado de oxidación +1.
El óxido y sulfato formado sobre la plata puede disolverse en ácido cítrico limpiándolo y formando citrato de plata.
La plata es uno de los siete metales conocidos desde la antigüedad. Se menciona en el libro del Génesis; y los montones de escoria hallados en Asia Menor e islas del mar Egeo, indican que el metal comenzó a separarse del plomo al menos cuatro milenios antes de Cristo.
No resulta difícil imaginar el efecto que hubo de producir en aquellos pobladores (que habían tallado y pulido la piedra, que encontraron y utilizaron el cobre y luego el estaño, llegando incluso a alear ambos por medio del fuego para obtener bronce) el descubrimiento de un metal raro y poco frecuente, de color blanco, brillo imperecedero e insensible al fuego que otros metales derretía. Tal asombro justificó la atribución al metal de singulares propiedades, de las que los demás metales carecían, salvo el oro claro está; pues ambos no eran sino regalos de la naturaleza, formados uno por el influjo de la Luna, y el otro por el del Sol. Los demás, viles metales, estaban sujetos a los cambios y transformaciones, que por los rudimentarios medios entonces disponibles podrían producirse; lejos, muy lejos, de la perfección de la plata y el oro. No es de extrañar que por ello surgiera la idea de la transmutación de los metales en un vano intento de perfeccionar aquellos viles metales y dando lugar a la aparición de las primeras doctrinas de la Alquimia. Particularmente adecuado parecía para tal propósito el mercurio en el que se observaba el aspecto y color de la plata, hasta tal punto que se le dio el nombre de hydrargyrum (plata líquida) de donde proviene su símbolo químico (Hg).
La plata, como el resto de los metales, sirvió para la elaboración de armas de guerra y luego se empleó en la manufactura de utensilios y ornamentos de donde se extendió al comercio al acuñarse las primeras monedas de plata y llegando a constituir la base del sistema monetario de numerosos países. En 1516 Juan Díaz de Solís descubrió en Sudamérica el mar Dulce que posteriormente Sebastián Caboto denominó Río de la Plata, creyendo que allí abundaba el precioso metal, y de donde tomará el nombre la Argentina. Años más tarde, el hallazgo de grandes reservas de plata en el Nuevo Mundo en Zacatecas y Potosí en Bolivia y su importación a Europa provocó un largo periodo de inflación que lejos de estancarse en España se difundió por Europa; el fenómeno fue estudiado por Earl Jefferson Hamilton que en 1934 publicó El tesoro americano y la revolución de los precios en España, 1501-1650.
Aleaciones y compuestos
La plata se alea fácilmente con casi todos los metales, excepto con el níquel que lo hace con dificultad y con el hierro y el cobalto con los que no se alea. Incluso a temperatura ordinaria forma amalgamas con mercurio.
El metal de aleación por excelencia es el cobre que endurece la plata hasta contenidos del 5% aunque se han utilizados platas con contenidos mayores de cobre. Las adiciones de cobre no alteran el color de la plata incluso hasta contenidos del 50%, aunque en éste caso el color se conserva en una capa superficial que al desgastarse mostrará una aleación de color rojizo, tanto más acusado cuanta mayor sea la cantidad de cobre. También se han usado aleaciones con cadmio en joyería ya que éste elemento le confiere a la aleación una ductilidad y maleabilidad adecuados para el trabajo del metal.
jose vidal ING petroquimica seccion I005 -
CI:22.984.980
carrera: petroquimica
seccion:I005
azufre
El azufre es un elemento químico de carácter no metálico, de color amarillo, es blando, frágil, ligero, que a su vez desprende un olor característico a huevo podrido y arde con llama de color azul desprendiendo dióxido de azufre. Es insoluble en agua pero se disuelve en disulfuro de carbono. Aunque también al mezclarse óxido de sulfuroso con agua produce lluvia ácida. Posee como valencias el +2, +4 y el +6.
El Azufre tiene como símbolo la letra S. El uso de los símbolos en la química y no solo en ésta sino también en la alquimia, tiene una función importante, la cual es representar de manera abreviada los cuerpos simples e incluso algunos compuestos conocidos en la antigüedad. Los primeros que iniciaron en éste arte combinaban sus doctrinas con la magia además de atribuir a los planetas, puesto que estos tenían una indudable influencia sobre las cosas y fenómenos de la Tierra, por ello, los metales eran conocidos por distintas divinidades planetarias.
El azufre ocupa el lugar 16 en abundancia entre los elementos químicos de la corteza terrestre, y está bastamente distribuido en la naturaleza, ya sea como azufre libre o como combinado. Existen depósitos de azufre libre o nativo, en sitios volcánicos. Igualmente existen depósitos subterráneos muy importantes. Son relativamente abundantes los sulfuros metálicos, tales como la pirita FeS2, pirita cúprica o calcopirita CuFeS2, galena PbS, blenda de cinc ZnS, sulfuros metálicos, como el sulfuro de plomo o galena, PbS; la esfalerita, ZnS; la calcopirita, (CuFeS2); el cinabrio, HgS; la estibina, Sb2S3, También se encuentra combinado con otros elementos formando sulfatos como la baritina, BaSO4; la celestina, SrSO4, y el yeso, CaSO4·2H2O.
El azufre a su vez está presente en muchos compuestos orgánicos, en productos, animales y vegetales: cebolla, ajo, mostaza, rábano silvestre, pelo, muchos aceites, huevos, proteínas, etc. El sulfuro de hidrógeno y sus productos de oxidación se encuentran en el agua de muchos manantiales sulfurosos. En estado libre se encuentra mezclado con rocas de yeso y pumita en zonas volcánicas, principalmente en Islandia, Sicilia, México y Japón, apareciendo a menudo como sublimados en las inmediaciones de orificios volcánicos. El azufre en estado libre puede formarse por la acción del aire sobre las piritas, o también depositarse por aguas sulfurosas calientes, en las cuales el sulfuro de hidrógeno se ha oxidado en contacto con la atmósfera
Efectos ambientales del Azufre
El azufre puede encontrarse en el aire en varias formas diferentes. Puede provocar irritaciones en los ojos y garganta de los animales, cuando la toma tiene lugar a través de la inhalación del azufre en su fase gaseosa. El azufre se aplica extensivamente en las industrias y es emitido al aire, debido a las limitadas posibilidades de destrucción de los enlaces de azufre que se aplican.
Los efectos dañinos del azufre en los animales son principalmente daños cerebrales, a través de un malfuncionamiento del hipotálamo, y perjudicar el sistema nervioso.
Pruebas de laboratorio con animales de prueba han indicado que el azufre puede causar graves daños vasculares en las venas del cerebro, corazón y riñones. Estos tests también han indicado que ciertas formas del azufre pueden causar daños fetales y efectos congénitos. Las madres pueden incluso transmitirles envenenamiento por azufre a sus hijos a través de la leche materna.
Por último, el azufre puede dañar los sistemas enzimáticos internos de los animales.
el azufre es elmento de mucha ayuda en el aspecto de las industrias pero hay que tener cuidado con este elemento porque cuasa mucho daño en el en ser humeno.
Osmiler Ruiz Pineda -
Torio
Nombre
Torio
Número atómico
90
Valencia
3
Estado de oxidación +4
Electronegatividad
1,3
Radio covalente (Å)
1,65
Radio iónico (Å)
0,95
Radio atómico (Å)
1,82
Configuración electrónica
[Rn]6d27s2
Primer potencial de ionización (eV)
-
Masa atómica (g/mol)
232,038
Densidad (g/ml)
11,7
Punto de ebullición (ºC)
3850
Punto de fusión (ºC)
1750
Descubridor
Jons Berzelius en 1828
Torio
Elemento químico, símbolo Th, número atómico 90. Es uno de los elementos de la serie de los actínidos. Es radiactivo con una vida media de aproximadamente 1.4 x 1010años.
Los compuestos de óxido de torio se utilizan en la producción de mantas de gas incandescentes. El óxido de torio se ha empleado también incorporado al tungsteno metálico, y sirve para producir filamentos para lámparas eléctricas. Se emplea en catalizadores para facilitar ciertas reacciones de química orgánica y tiene aplicaciones especiales como material cerámico de alta temperatura. El metal o sus óxidos se utilizan en algunas lámparas electrónicas, fotoceldas y electrodos especiales para soldadura. El torio tiene aplicaciones importantes como agente de aleación en algunas estructuras metálicas. Tal vez el empleo más importante del torio metálico, aparte del campo nuclear, esté en la tecnología del magnesio. En un reactor nuclear, el torio puede ser convertido en uranio 233, que es un combustible atómico. Se ha estimado que la energía que se puede obtener de las reservas mundiales de torio es tan grande como la energía combinada que pueden proporcionar todo el uranio, el carbón y el petróleo del mundo. La monazita, el mineral de torio más común y el más importante desde el punto de vista comercial, está ampliamente distribuida en la naturaleza.
La monazita se obtiene principalmente como una arena, que se separa de otras arenas por medios físicos o mecánicos.
El torio tiene un peso atómico de 232.038. La temperatura a la cual se funde el torio puro no se conoce con certeza; se cree que es cercana a 1750ºC (3182ºF). El torio metálico de buena calidad es relativamente suave y dúctil. Puede ser conformado fácilmente por cualesquiera de las operaciones comunes para trabajar los metales. El metal masivo es de color plateado, pero pierde el brillo por una exposición prolongada a la atmósfera; el torio finamente dividido tiende a ser pirofórico en el aire.
Todos los elementos no metálicos, excepto los gases raros, forman compuestos binarios con él. Con pocas excepciones, el torio exhibe una valencia de 4+ en todas sus sales. Químicamente, tiene algunas semejanzas con el zirconio y el hafnio. El compuesto más soluble del torio es el nitrato, el cual, como se prepara generalmente, parece tener la fórmula Th(NO3)4 . 4H2O. El óxido más común del torio es ThO2, toria. El torio se combina con los halógenos para formar gran variedad de sales. El sulfato de torio se puede obtener en forma anhidra o como cierto número de hidratos. Se conocen bien los carbonatos, fosfatos, yodatos, cloratos, cromatos, molibdatos y otras sales inorgánicas de torio. El torio forma también sales con muchos ácidos orgánicos, de los cuales el oxalato insoluble en agua Th(C2O4)2 6H2O, es importante en la preparación de compuestos puros de torio.
Efectos del Torio sobre la salud
Las personas siempre estarán expuestas a pequeñas cantidades de torio a través del aire, la comida y el agua, porque se encuentra casi en cualquier lugar en La Tierra.
Todo el mundo absorbemos algo de torio a través de la comida o el agua que bebemos, y las cantidades en el aire son tan pequeñas, que la toma a través del aire normalmente puede ser ignorada.
Grandes cantidades incontroladas de torio pueden ser encontradas cerca de vertederos peligrosos donde el torio no fue vertido de acuerdo con los procedimientos adecuados. Las personas que viven cerca de estos lugares de vertidos peligrosos pueden estar expuestos a más torio de lo normal porque respiran polvo arrastrado por el viento y porque termina en la comida que es cultivada cerca del lugar.
Las personas que trabajan en las industrias o laboratorios mineros, molineros o del torio también pueden experimentar exposiciones al torio que superan la exposición natural.
Las cantidades de torio en el medio ambiente pueden verse aumentadas accidentalmente debido a escapes accidentales de las plantas procesadoras de torio.
Respirar torio en el lugar de trabajo puede incrementar las posibilidades de desarrollar enfermedades de pulmón y cáncer de pulmón y páncreas muchos años después de la exposición. El torio tiene la habilidad de cambiar el material genético. Las personas a las que les ha sido inyectado torio para los rayos X especiales pueden desarrollar enfermedades del hígado.
El torio es radiactivo y puede ser almacenado en los huesos. Debido a ésto tiene la habilidad de causar cáncer de huesos muchos años después de que la exposición haya tenido lugar.
La respiración de grandes cantidades de torio puede ser letal. Las personas a menudo mueren de envenenamiento por metales cuando se someten a una exposición excesiva.
Efectos ambientales del Torio
Estabilidad ambiental: El torio reaccionará lentamente con el agua, el oxígeno y otros compuestos para formar una variedad de compuestos del torio.
Efectos del material en plantas y animales: Debido al tamaño del producto, no se esperan efectos ambientales inusuales de estos productos; sin embargo, grandes escapes de torio pueden ser dañinos para las plantas y animales afectados.
Efectos de los productos químicos en la vida acuática: Debido al tamaño del producto y a la forma del producto, estos productos no se puede anticipar que causen efectos adversos en la vida acuática; sin embargo, grandes escapes de torio en un cuerpo de agua pueden ser dañinos para las plantas acuáticas y los animales.
La eliminación de los vertidos debe realizarse de acuerdo con las adecuadas regulaciones federales, estatales y locales.
Yessica Flores Ing. Civil I-003 2do semestre -
Mercurio
Número atómico
80
Valencia
1,2
Estado de oxidación
+2
Electronegatividad
1,9
Radio covalente (Å)
1,49
Radio iónico (Å)
1,10
Radio atómico (Å)
1,57
Configuración electrónica
[Xe]4f145d106s2
Primer potencial
de ionización (eV)
10,51
Masa atómica (g/mol)
200,59
Densidad (g/ml)
16,6
Punto de ebullición (ºC)
357
Punto de fusión (ºC)
-38,4
Descubridor
Los antiguos
Mercurio
Elemento químico, símbolo Hg, número atómico 80 y peso atómico 200.59. es un líquido blanco plateado a temperatura ambiente (punto de fusión -38.4ºC o -37.46ºF); ebulle a 357ºC (675.05ºF) a presión atmosférica. Es un metal noble, soluble únicamente en soluciones oxidantes. El mercurio sólido es tan suave como el plomo. El metal y sus compuestos son muy tóxicos. El mercurio forma soluciones llamadas amalgamas con algunos metales (por ejemplo, oro, plata, platino, uranio, cobre, plomo, sodio y potasio).
En sus compuestos, el mercurio se encuentra en los estados de oxidación 2+, 1+ y más bajos; por ejemplo, HgCl2, Hg2Cl2 o Hg3(AsF6)2. A menudo los átomos de mercurio presentan dos enlaces covalentes; por ejemplo, Cl-Hg-Cl o Cl-Hg-Hg-Cl. Algunas sales de mercurio(II), por ejemplo, Hg(NO3)2 o Hg(ClO4)2, son muy solubles en agua y por lo general están disociadas. Las soluciones acuosas de estas sales reaccionan como ácidos fuertes a causa de la hidrólisis que ocurre. Otras sales de mercurio(III), como HgCl2 o Hg(Cn)2, también se disuelven en agua, pero en solución sólo están poco disociadas. Hay compuestos en que los átomos de mercurio están directamente enlazados a átomos de carbono o de nitrógeno; por ejemplo, H3C-Hg-CH3 o H3C-CO-NH-Hg-NH-CO-CH3. En complejos, como K2(HgI4), a menudo tiene tres o cuatro enlaces.
El mercurio metálico se usa en interruptores eléctricos como material líquido de contacto, como fluido de trabajo en bombas de difusión en técnicas de vacío, en la fabricación de rectificadores de vapor de mercurio, termómetros, barómetros, tacómetros y termostatos y en la manufactura de lámparas de vapor de mercurio. Se utiliza en amalgamas de plata para empastes de dientes. Los electrodos normales de calomel son importantes en electroquímica; se usan como electrodos de referencia en la medición de potenciales, en titulaciones potenciométricas y en la celda normal de Weston.
El mercurio se encuentra comúnmente como su sulfuro HgS, con frecuencia como rojo de cinabrio y con menos abundancia como metalcinabrio negro. Un mineral menos común es el cloruro de mercurio(I). A veces los minerales de mercurio contienen gotas pequeñas de mercurio metálico.
La tensión superficial de mercurio líquido es de 484 dinas/cm, seis veces mayor que la del agua en contacto con el aire. Por consiguiente, el mercurio no puede mojar ninguna superficie con la cual esté en contacto. En aire seco el mercurio metálico no se oxida, pero después de una larga exposición al aire húmedo, el metal se cubre con una película delgada de óxido. No se disuelve en ácido clorhídrico libre de aire o en ácido sulfúrico diluido, pero sí en ácidos oxidantes (ácido nítrico, ácido sulfúrico concentrado y agua regia).
milianyer Landaeta Ing.Civil 003 2 semestre -
Nombre
Litio
Número atómico
3
Valencia
1
Estado de oxidación
+1
Electronegatividad
1,0
Radio covalente (Å)
1,34
Radio iónico (Å)
0,60
Radio atómico (Å)
1,55
Configuración electrónica
1s22s1
Primer potencial de ionización (eV)
5,41
Masa atómica (g/mol)
6,941
Densidad (g/ml)
0,53
Punto de ebullición (ºC)
1330
Punto de fusión (ºC)
180,5
victoria vasquez -
ing.civil 003-D
Elemento químico, Br, número atómico 35 y peso atómico 79.909, por lo común existe como Br2; líquido de olor intenso e irritante, rojo oscuro y de bajo punto de ebullición, pero de alta densidad. Es el único elemento no metálico líquido a temperatura y presión normales. Es muy reactivo químicamente; elemento del grupo de los halógenos, sus propiedades son intermedias entre las del cloro y las del yodo.
Los estados de valencia más estables de las sales de bromo son 1- y 5+, aunque también se conocen 1+, 3+ y 7+. Dentro de amplios límites de temperatura y presión, las moléculas en el líquido y el vapor son diatómicas Br2, con un peso molecular de 159.818. Hay dos isótopos estables (79Br y 81Br) que existen en la naturaleza en proporciones casi idénticas, de modo que el peso atómico es de 79.909. Se conocen también varios radioisótopos. La solubilidad del bromo en agua a 20ºC (68ºF) es de 3.38 a/100 g (3.38 oz/100 oz) de solución, pero ésta se incrementa fuertemente en presencia de sus sales y de ácido bromhídrico. La capacidad de este elemento inorgánico para disolverse en disolventes orgánicos es de importancia considerable en sus reacciones. A pesar de que la corteza terrestre contiene de 1015 a 1016 toneladas de bromo, el elemento está distribuido en forma amplia y se encuentra en concentraciones bajas en forma de sales. La mayor parte del bromo recuperable se halla en la hidrosfera. El agua de mar contiene en promedio 65 partes por millón (ppm) de bromo. Las otras fuentes principales en Estados Unidos son salmueras subterráneas y lagos salados, con producción comercial en Michigan, Arkansas y California.
Los bromuros orgánicos son a menudo aplicados como agentes desinfectantes y protectores, debido a sus efectos perjudiciales para los microorganismos. Cuando se aplican en invernaderos y en campos de cultivo pueden ser arrastrados fácilmente hasta las aguas superficiales, lo que tiene efectos muy negativos para la salud de las daphnia, peces, langostas y algas.
Los bromuros orgánicos son también perjudiciales para los mamíferos, especialmente cuando se acumulan en los cuerpos de sus presas. Los efectos más importantes sobre los animales son daños nerviosos y daños en el ADN, lo que puede aumentar las probabilidades de desarrollar cáncer.
La toma de bromuro orgánico tiene lugar a través de la comida, de la respiración y a través de la piel.
Los bromuros orgánicos no son muy biodegradables; cuando son descompuestos se forman bromuros inorgánicos. Éstos pueden dañar el sistema nervioso si son absorbidos en grandes dosis. Ha ocurrido en el pasado que los bromuros orgánicos terminaron en la comida del ganado. Miles de vacas y cerdos tuvieron que ser sacrificados para prevenir el contagio a los humanos. El ganado sufrió de síntomas tales como daños en el hígado, pérdida de visión y disminución del crecimiento, reducción de la inmunidad, decrecimiento de la producción de leche y esterilidad y malformaciones fetales.
Nombre
Bromo
Número atómico
35
Valencia
+1,-1,3,5,7
Estado de oxidación
-1
Electronegatividad
2,8
Radio covalente (Å)
1,14
Radio iónico (Å)
1,95
Radio atómico (Å)
-
Configuración electrónica
[Ar]3d104s24p5
Primer potencial
de ionización (eV)
11,91
Masa atómica (g/mol)
79,909
Densidad (g/ml)
3,12
Punto de ebullición (ºC)
58
Punto de fusión (ºC)
-7,2
Descubridor
Anthoine Balard en 1826
reina gonzalez ing petroquimica semestre 2 seccion ioo5d -
Nombre Radio
Número atómico 88
Valencia 2
Electronegatividad 0,9
Radio covalente (Å) -
Radio iónico (Å)
(estado de oxidación) 1,40 (+2)
Radio atómico (Å) -
Configuración electrónica [Rn]7s2
Primer potencial
de ionización (eV) 5,28
Masa atómica (g/mol) (226)
Densidad (g/ml) 5,0
Punto de ebullición (ºC) -
Punto de fusión (ºC) 700
Elemento químico, símbolo Ra, de número atómico 88. El radio es un elemento radiactivo raro, encontrado en minerales de uranio en proporción de una parte por aproximadamente 3 millones de partes de uranio. Desde el punto de vista químico, el radio es un metal alcalinotérreo y tiene propiedades muy semejantes a las del bario. Biológicamente, el radio se concentra en los huesos al reemplazar al calcio y, tras una irradiación prolongada, causa anemia y neoplasias cancerosas. Dado que las radiaciones del radio y de sus productos de descomposición destruyen preferentemente los tejidos malignos, el radio se ha utilizado para detener el crecimiento del cáncer. En su aplicación terapéutica, los compuestos de radio puro se sellan en tubos o agujas; también el radón, producto gaseoso de descomposición del radio, se bombea en tubos pequeños. El empleo del radio en pinturas luminosas para relojes de pared o pulsera y esferas de medida, así como en señales visibles en la oscuridad se basa en su radiación alfa que golpea un tubo de centelleo, como el de sulfuro de zinc.
Se conocen 13 isótopos del radio; todos son radiactivos; cuatro se encuentran en la naturaleza y el resto se produce sintéticamente. Sólo el 226Ra es tecnológicamente importante. Se encuentra ampliamente distribuido en al naturaleza, por lo regular en cantidades mínimas. La fuente más concentrada es la pecblenda (uraninita).
Cuando son de preparación reciente, casi todos los compuestos de radio son blancos, pero se decoloran permanentemente a causa de su intensa radiación. Las sales de radio ionizan la atmósfera que los rodea, por eso parece que emiten un resplandor azul. Los compuestos de radio descargan los electroscopios, velan las placas fotográficas protegidas de la luz y producen fosforescencia y fluorescencia en ciertos compuestos inorgánicos como el sulfuro de zinc. El espectro de emisión de los compuestos de radio se parece al de otros alcalinotérreos; los halogenuros de radio imparten color rojo carmín a la llama.
su distribucion electronica es
Radio (z: 18)
1s2 2s2 2p6 3s2 3p6
dionna medina -
El manganeso es un metal de transición blanco grisáceo, parecido al hierro. Es un metal duro y muy frágil, refractario y fácilmente oxidable. El manganeso metal puede ser ferromagnético, pero sólo después de sufrir un tratamiento especial.
Sus estados de oxidación más comunes son 2+, 3+, 4+, 6+ y 7+, aunque se han encontrado compuestos con todos los números de oxidación desde 1+ a 7+; los compuestos en los que el manganeso presenta estado de oxidación 7+ son agentes oxidantes muy enérgicos. Dentro de los sistemas biológicos, el catión Mn2+ compite frecuentemente con el Mg2+. Se emplea sobre todo aleado con hierro en aceros y en otras aleaciones.
Se ha encontrado dióxido de manganeso, MnO2, en pinturas rupestres (dando un color negro). También se han utilizado a lo largo de la historia, por ejemplo por los egipcios y los romanos, compuestos de manganeso para decolorar el vidrio o bien darle color. Asimismo se ha encontrado manganeso en la minas de hierro utilizadas por los espartanos, y se piensa que tal vez sea debido a esto la especial dureza de sus aceros.
En el siglo XVII, el químico alemán Glauber, produjo por primera vez permanganato, un reactivo de laboratorio bastante utilizado. A mediados del siglo XVIII, el dióxido de manganeso se empleó para la producción de cloro. El químico sueco Scheele fue el primero que descubrió que el manganeso era un elemento, pero fue Johan Gottlieb Gahn quien lo aisló por reducción del dióxido con carbono.
A principios del siglo XIX se comenzó a probar el manganeso en aleaciones de acero. En 1816 se comprobó que endurecía al acero, sin hacerlo más frágil
El permanganato de potasio, KMnO4, es un reactivo de laboratorio muy común debido a sus propiedades oxidantes.
El dióxido de manganeso, MnO2 se emplea como despolarizador en pilas secas. También se puede usar para decolorar vidrio que presente color verde debido a la presencia de trazas de hierro. Este óxido también se emplea para dar color amatista al vidrio, y es responsable del color de la amatista (una variedad del cuarzo). Además, se utiliza en la producción de cloro y oxígeno. Algunas monedas de Aluminio contienen Manganeso como aleación.
ranald ojeda -
C.I: 20513485
SECCION: I003 ING CIVIL
Uranio
Saltar a navegación, búsqueda
Para otros usos de este término, véase Uranio (desambiguación).
Protactinio - Uranio - Neptunio
Nd
U
Tabla completa
General
Nombre, símbolo, número
Uranio, U, 92
Serie química
Actínidos
periodo, bloque
8 , f
Densidad, dureza Mohs
19.050 kg/m3, sin datos
Apariencia
Metal blanco plateado
Propiedades atómicas
Masa atómica
238,0289 u
Radio medio 175 pm
Radio atómico calculado
Sin datos
Radio covalente
Sin datos
Radio de Van der Waals
186 pm
Configuración electrónica
[Rn]7s25f36d1
Estados de oxidación (óxido)
5 (base débil)
Estructura cristalina
Ortorrómbica
Propiedades físicas
Estado de la materia
Sólido (__)
Punto de fusión
1405 K (1132°C)
Punto de ebullición
4404 K (4131erC)
Entalpía de vaporización
477 kJ/mol
Entalpía de fusión
15,48 kJ/mol
Presión de vapor
Sin datos
Velocidad del sonido
3155 m/s a 293,15 K
Información diversa
Electronegatividad
1,38 (Pauling)
Calor específico
120 J/(kgK)
Conductividad eléctrica
3,8 × 106 m1Ω1
Conductividad térmica
27,6 W/(mK)
1er potencial de ionización
597,6 kJ/mol
2° potencial de ionización 1420 kJ/mol
Isótopos más estables
iso.
AN
Periodo de semidesintegración
MD
ED MeV
PD
U232 Sintético
68,9 a
α & FE
5.414 Th228
U233 Sintético 159200 a
FE & α 4,909 Th229
U234 0,0054% 245500 a
FE & α 4,859 Th230
U235
0,7204% 7,038 × 108 a
SF & α 4,679 Th231
U236 Sintético 2,342 × 107 a
FE & α 4,572 Th232
U238 99,2742% 4.51 × 109 a
FE & α 4,270 Th234
Valores en el SI y en condiciones normales
(0 °C y 1 atm), salvo que se indique lo contrario.
Calculado a partir de distintas longitudes
de enlace covalente, metálico o iónico.
El uranio es un elemento químico metálico de color plateado-grisáceo de la serie de los actínidos, su símbolo químico es U y su número atómico es 92. Por ello posee 92 protones y 92 electrones, con una valencia de 6. Su núcleo puede contener entre 141 y 146 neutrones, sus isótopos más abundantes son el U-238 que posee 146 neutrones y el U-235 con 143 neutrones. El Uranio tiene el mayor peso atómico de entre todos los elementos que se encuentran en la naturaleza. El Uranio es aproximadamente un 70% más denso que el plomo, aunque menos denso que el oro o el wolframio. Es levemente radioactivo. Fue descubierto en 1789 por M. H. Klaproth que lo llamó así en el honor del planeta Urano que acababa de ser descubierto en 1781.
En la naturaleza se presenta en muy bajas concentraciones (unas pocas partes por millón o ppm) en rocas, tierras, agua y los seres vivos. Para su uso el Uranio debe ser extraído y concentrado a partir de minerales que lo contienen como por ejemplo la uranita (ver minería del Uranio). Las rocas son tratadas químicamente para separar el uranio, convirtiéndolo en compuestos químicos de uranio. El residuo se denomina estéril. Esos estériles contienen las mismas sustancias radiactivas que poseía el mineral original y que no fueron separadas, como el radio, el torio o el potasio.
El uranio natural está formado por tres tipos de isótopos: uranio-238 (238U), uranio-235 (235U) y uranio-234 (234U). De cada gramo de uranio natural el 99,284 % de la masa es uranio-238, el 0,711% uranio-235,[1] y 0,0085% uranio-234. La relación Uranio-238/Uranio-235 es constante en la corteza terrestre, salvo ciertas excepciones.
El Uranio decae muy lentamente emitiendo una partícula alfa. El periodo de semidesintegración del uranio-238 es aproximadamente 4.470 millones de años y el del uranio-235 es 704 millones de años,[2] lo que los convierte en útiles para estimar la edad de la Tierra (véase fechado mediante Uranio-Torio, fechado mediante Uranio-Plomo y fechado mediante Uranio-Uranio). Muchos usos contemporaneos del Uranio hacen uso de estas propiedades nucleares únicas. El Uranio-235 se distingue por ser el único elemento que se encuentra en la naturaleza que es un isótopo físil. El Uranio-238 es fisionable por neutrones rápidos, y también es un material fértil (que puede transmutarse en un reactor nuclear en plutonio-239 que es físil). Es posible producir el isótopo físil artificial, Uranio-233, a partir de torio natural, lo que desempeña un rol importante en la tecnología nuclear. Mientras que el Uranio-238 posee una pequeña probabilidad de fisión espontánea o al ser bombardeado por neutrones rápidos, el uranio-235 posee una mayor probabilidad de fisionarse al ser bombardeado por neutrones térmicos, por lo que es la reacción principalmente responsable por la generación de calor en un reactor nuclear, y es la principal fuente de material físil para las armas nucleares. Ambos usos son posibles por la capacidad del uranio de sostener una reacción nuclear en cadena. El uranio empobrecido (uranio-238) es utilizado en penetradores de energía cinética y protecciones para vehículos blindados.[3]
El 235U se utiliza como combustible en centrales nucleares y en algunos diseños de armamento nuclear. Para producir combustible, el uranio natural es separado en dos porciones. La porción combustible tiene más 235U que lo normal, denominándoseuranio enriquecido, mientras que la porción sobrante, con menos U235 que lo normal, se llama uranio empobrecido. El uranio natural, enriquecido o empobrecido es químicamente idéntico. El uranio empobrecido es el menos radiactivo y el enriquecido el más radiactivo.
En el año 2009, la sonda japonesa SELENE descubrió indicios por primera vez de uranio en la Luna.
Contenido
[ocultar]
1 Origen
2 Uso
3 Efectos nocivos para la salud
4 Referencias
5 Enlaces externos
Origen
Junto con todos los elementos con pesos atómicos superiores al del hierro, el uranio se origina de forma natural durante las explosiones de las supernovas. El proceso físico determinante en el colapso de una supernova es la gravedad. Los valores tan elevados de gravedad que se dan en las supernovas es lo que genera las capturas neutrónicas que dan lugar a los átomos más pesados, entre ellos el uranio y el protactinio.
Uso
El principal uso del uranio en la actualidad es como combustible para los reactores nucleares que producen el 17% de la electricidad obtenida en el mundo. Para ello el Uranio es enriquecido aumentando la proporción del isótopo U235 desde el 0,71% que presenta en la naturaleza hasta calores en el rango 2-3%. El uranio empobrecido es usado en la producción de municiones perforantes y blindajes de alta resistencia. Otros usos incluyen;
Por su alta densidad, se utiliza el uranio en la construcción de estabilizadores para aviones, satélites artificiales y veleros.
Se ha utilizado Uranio como agregado para la creación de cristales de tonos verdes.
El largo periodo de semidesintegración del isótopo 238U se utiliza para estimar la edad de la Tierra.
El 238U se convierte en plutonio en los reactores reproductores. El plutonio puede ser usado en reactores o en armas nucleares.
Algunos accesorios luminosos utilizan uranio, del mismo modo que lo hacen algunos químicos fotográficos (nitrato de uranio) [
El uranio en estado metálico es usado como blanco para generar rayo X.
Su alto peso atómico hace que el 238U pueda ser utilizado como un eficaz blindaje contra las radiaciones de alta penetración.
Los fertilizantes de fosfato pueden contener un contenido en uranio natural alto, cuando el mineral con el que se fabrican tiene un contenido de uranio también alto.
Efectos nocivos para la salud
El uranio en cualquiera de sus formas (natural, enriquecido o empobrecido), al ser un metal pesado, posee una cierta toxicidad, pudiendo afectar al sistema renal, dependiendo los efectos de la cantidad incorporada al organismo.
Además el uranio es el padre de una de las cadenas naturales, siendo uno de sus hijos radiactivos el radón-222, considerado cancerígeno y con sinergias con el humo del taaco.
robert chacon -
Nombre
Californio
Número atómico
98
Valencia
3
Estado de oxidación -
Electronegatividad
Radio covalente (Å)
-
Radio iónico (Å)
-
Radio atómico (Å)
-
Configuración electrónica
[Rn]5f96d17s2
Primer potencial
de ionización (eV)
-
Masa atómica (g/mol)
251
Densidad (g/ml)
-
Punto de ebullición (ºC)
-
Punto de fusión (ºC)
-
Descubridor
G.T. Seaborg en 1950
El californio metálico es muy volátil y destila a temperaturas del orden de 1100-1200ºC (2010-2190ºF). Es químicamente reactivo y existe en tres diferentes modificaciones cristalinas entre la temperatura ambiente y su punto de fusión 900ºC (1600ºF)
leonardo servet -
El sodio está presente en grandes cantidades en el océano en forma iónica. También es un componente de muchos minerales y un elemento esencial para la vida.
Al igual que otros metales alcalinos el sodio es un metal blando, ligero y de color plateado que no se encuentra libre en la naturaleza. El sodio flota en el agua descomponiéndola, desprendiendo hidrógeno y formando un hidróxido. En las condiciones apropiadas reacciona espontáneamente en el agua. Normalmente no arde en contacto con el aire por debajo de 40 °C).
El sodio metálico se emplea en síntesis orgánica como agente reductor. Es además componente del cloruro de sodio necesario para la vida. Otros usos son:
En aleaciones antifricción (oro).
En la fabricación de desodorantes (en combinación con ácidos grasos).
En la purificación de metales fundidos.
La aleación Na K, es un material empleado para la transferencia de calor además de desecante para disolventes orgánicos y como reductor. A temperatura ambiente es líquida. El sodio también se emplea como refrigerante.
Aleado con plomo se emplea en la fabricación de aditivos detonantes para las gasolinas.
Se emplea también en la fabricación de células fotoeléctricas.
Iluminación mediante lámparas de vapor de sodio.
Los óxidos NaO2 generados por combustión controlada con oxígeno se utilizan para intercambiar el dióxido de carbono por oxígeno y regenerar así el aire en espacios cerrados (p. ej. en submarinos)
Papel biológico
El catión sodio (Na+) tiene un papel fundamental en el metabolismo celular, por ejemplo, en la transmisión del impulso nervioso (mediante el mecanismo de bomba de sodio-potasio). Mantiene el volumen y la osmolaridad. Participa, además del impulso nervioso, en la contracción muscular, el equilibrio ácido-base y la absorción de nutrientes por las membranas.
La concentración plasmática de sodio es en condiciones normales de 137 - 145 mmol/L. El aumento de sodio en la sangre se conoce como hipernatremia y su disminución hiponatremia.
Pedro Sanchez, C.I. 21.238.868, Ing. Petroquimica I-005, II Semestre -
Un átomo de oxígeno combinado con dos de hidrógeno forman una molécula de agua.
Oxígeno
Nitrógeno ← Oxígeno → Flúor
-
8 O
O
S
Tabla completa Tabla extendida
Información general
Nombre, símbolo, número Oxígeno, O, 8
Serie química No metales
Grupo, período, bloque 16, 2, p
Densidad 1,429 kg/m3
Apariencia Incoloro
N° CAS {{{CAS}}}
N° EINECS {{{EINECS}}}
Propiedades atómicas
Densidad 15,9994 u
Radio medio {{{radio_medio}}} pm
Radio atómico (calc) 60 (48) pm (Radio de Bohr)
Radio covalente 73 pm
Radio de van der Waals 152 pm
Configuración electrónica 1s22s22p4
Electrones por nivel de energía {{{electrones_por_nivel}}}
Estado(s) de oxidación -2, -1 (neutro)
Óxido {{{óxido}}}
Estructura cristalina cúbica
Propiedades físicas
Estado ordinario Gas (paramagnético)
Punto de fusión 50,35 K
Punto de ebullición 90,18 K
Punto de inflamabilidad {{{P_inflamabilidad}}} K
Entalpía de vaporización 3,4099 kJ/mol
Entalpía de fusión 0,22259 kJ/mol
Presión de vapor {{{presión_vapor}}}
Temperatura crítica {{{T_crítica}}} K
Presión crítica {{{P_crítica}}} Pa
Volumen molar 17,36×10-3 m3/mol
Velocidad del sonido 317,5 m/s a 20 °C
Varios
Electronegatividad (Pauling) 3,44
Calor específico 920 J/(kg·K)
Conductividad eléctrica S/m
Conductividad térmica 0,026 74 W/(m·K)
1.ª Energía de ionización 1313,9 kJ/mol
2.ª Energía de ionización 3388,3 kJ/mol
3.ª Energía de ionización 5300,5 kJ/mol
4.ª Energía de ionización 7469,2 kJ/mol
5.ª Energía de ionización {{{E_ionización5}}} kJ/mol
6.ª Energía de ionización {{{E_ionización6}}} kJ/mol
7.ª Energía de ionización {{{E_ionización7}}} kJ/mol
8.ª Energía de ionización {{{E_ionización8}}} kJ/mol
9.ª Energía de ionización {{{E_ionización9}}} kJ/mol
10.ª Energía de ionización {{{E_ionización10}}} kJ/mol
Isótopos mas estables
iso AN Periodo MD Ed PD
MeV
16O 99,762% estable con 8 neutrones
17O 0,038% estable con 9 neutrones
18O 0,2% estable con 10 neutrones
Nota: unidades según el SI y en CNPT, salvo indicación contraria.
su distribucion electronica es esta:
elemento = Oxigeno
O = 8 e.
1s2, 2s2, 2p4
lilibeth martinez -
Platino
Número atómico
78
Valencia
2,4
Estado de oxidación
+2
Electronegatividad
2,2
Radio covalente (Å)
1,28
Radio iónico (Å)
0,52
Radio atómico (Å)
1,38
Configuración electrónica
[Xe]4f145d96s1
Primer potencial de ionización (eV)
9,03
Masa atómica (g/mol)
195,09
Densidad (g/ml)
21,4
Punto de ebullición (ºC)
4530
Punto de fusión (ºC)
1769
Descubridor
Julius Scaliger en 1735
Platino
Es un metal noble blanco, blando y dúctil. Los metales del grupo del platino ( platino, paladio, iridio, rodio , osmio y rutenio) se encuentran ampliamente distribuidos sobre la tierra, pero su dilución extrema imposibilita su recuperación, excepto en circunstancias especiales. Los metales del grupo del platino se utilizan mucho en el campo de la química a causa de su actividad catalítica y de su baja reactividad. Como catalizador, el platino se emplea en las reacciones de hidrogenación, deshidrogenación, isomerización, ciclización, deshidratación, deshalogenación y oxidación.
El platino no es afectado por la atmósfera aun en ambientes industriales con contenido de azufre. Conserva su brillantez y no exhibe película de óxido cuando se calienta, aunque se forma una película fina adherente debajo de los 450ºC (842ºF). El hidrógeno u otras atmósferas reductoras no son peligrosas para el platino a temperaturas elevadas. El platino puede ser maquinado en alambres finos y láminas delgadas y, por procesos especiales, en alambres extremadamente finos.
El platino puede obtenerse en forma esponjosa por descomposición térmica del cloroplatinato de amonio o al reducirlo de una solución acuosa. En esta forma muestra un alto poder de absorción respecto a los gases, especialmente oxígeno, hidrógeno y monóxido de carbono. La alta actividad catalítica del platino está relacionada directamente con esta propiedad. El platino posee una fuerte tendencia a formar compuestos de coordinación.
El dióxido de platino, PtO2, es un compuesto castaño oscuro insoluble, conocido comúnmente como catalizador de Adams. El cloruro de platino(II), PtCl2, es un sólido verde oliva insoluble en agua. El ácido cloroplatínico, H2PtCl6, es el compuesto de platino más importante.
Efectos del Platino sobre la salud
El Platino es un metal noble. Las concentraciones de platino en el suelo, agua y aire son mínimas. en Sur África, la Unión Soviética y Estados Unidos. El Platino es usado como componente de varios productos metálicos, como son los electrodos y este puede ser usado como catalizador en un número de reacciones químicas. Los enlaces del platino son a menudo aplicados en medicina para curar el cáncer. Los efectos sobre la salud del Platino están fuertemente ligados a la clase de enlace que estos forman y el nivle de exposición y la inmunidad de la persona que es expuesta.
Luz Briceño -
el oro
simbolo:Au
Oro
Elemento químico, símbolo Au, número atómico 79 y peso atómico 196.967; es un metal muy denso, blando y de color amarillo intenso. El oro se clasifica como metal pesado y noble; en el comercio es el más común de los metales preciosos. El cobre, la plata y el oro están en el mismo grupo en la tabla periódica. La fuente del símbolo químico, Au, es su nombre en latín aurum (amanecer radiante). Hay sólo un isótopo estable del oro, con número de masa 197.
Usos: Cerca de tres cuartas partes de la producción mundial del oro se consume en joyería. Sus aplicaciones industriales, especialmente en electrónica, consumen 10-15%. El remanente está dividido entre los empleos médicos y dentales, acuñación y reservas para el gobierno y particulares. Las monedas y demás objetos decorativos de oro son en realidad aleaciones porque el metal es muy blando (2.5-3 en la escala de Mohs) para ser útil con un manejo frecuente.
El 198Au radiactivo se utiliza en radiaciones medicinales, en diagnóstico y en algunas aplicaciones industriales como trazador. También se usa como trazador en el estudio del movimiento de sedimentos sobre el fondo oceánico y en los alrededores de los puertos. Las propiedades del oro hacia la energía radiante han permitido el desarrollo de reflectores eficientes para calentadores infrarrojos y hornos, así como para retención y enfoque de calor en procesos industriales.
Localización: El oro se encuentra distribuido por todo el mundo, pero es muy escaso, de tal suerte que es un elemento raro. El agua de mar contiene concentraciones bajas de oro del orden de 10 partes de oro por billón de partes de agua. En el plancton o en el fondo marino se acumulan concentraciones superiores. En la actualidad, no existen procesos económicos adecuados para la extracción del oro marino. El oro metálico, o natural, y varios minerales telúricos son las únicas formas de oro presentes en la Tierra. El oro natural existe en las rocas y minerales de otros metales, especialmente en el cuarzo y la pirita, o puede estar disperso en arenas y gravas (oro de aluvión).
Propiedades: La densidad del oro es 19,3 veces la del agua a 20ºC (68ºF), tal que 1 m3 de oro pesa cerca de 19 000 kg (1 pie3, unas 1200 libras). Las masas del oro, al igual que otros metales preciosos, se miden en la escala Troy, la cual contiene 12 onzas por libra. Se funde a 1063ºC (1947.97ºF) y ebulle a 2970ºC (5180ºF). Es algo volátil por debajo de su punto de ebullición. Es un buen conductor de calor y electricidad. Es el metal más dúctil y maleable. Pueden hacerse láminas transparentes, con espesor de 0.00001 mm con facilidad o estirarlo en alambres con pesos de 0.5 mg/m. Su calidad se expresa en la escala de finura como partes de oro puro por mil partes de metal total, o en la escala de quilate como partes de oro puro por 24 partes de metal total. El oro se disuelve con facilidad en mercurio para formar amalgamas. Es uno de los metales menos reactivos químicamente. No pierde lustre, ni se quema al aire. Es inerte en soluciones fuertemente alcalinas y en todos los ácidos puros, menos el ácido selénico.
Compuestos: El oro puede tener valencia 1+ o 3+ en sus compuestos. La tendencia a formar complejos es tan fuerte que todos los compuestos de oxidación 3+ son complejos. Los compuestos del estado de oxidación 1+ no son muy estables y tienden a oxidarse al estado 3+ o reducirse a oro metálico. Todos los compuestos de cualquier estado de oxidación se reducen con facilidad.
En sus complejos el oro forma enlaces más fácilmente y más estables con los halógenos y el azufre, menos estables con oxígeno y fósforo y muy débiles con nitrógeno. Los enlaces entre oro y carbono son normalmente estables, como en los complejos de cianuro y varios compuestos orgánicos.
joel pereira C.I: 21199697 I005D ing. petroquimica II semestres -
simbolo: CU (del latín cuprum)
numero atomico: 29
Se trata de un metal de transición de color rojizo y brillo metálico que, junto con la plata y el oro, forma parte de la llamada familia del cobre, caracterizada por ser los mejores conductores de electricidad. Gracias a su alta conductividad eléctrica, ductilidad y maleabilidad, se ha convertido en el material más utilizado para fabricar cables eléctricos y otros componentes eléctricos y electrónicos.
El cobre forma parte de una cantidad muy elevada de aleaciones que generalmente presentan mejores propiedades mecánicas, aunque tienen una conductividad eléctrica menor. Las más importantes son conocidas con el nombre de bronces y latones. Por otra parte, el cobre es un metal duradero porque se puede reciclar un número casi ilimitado de veces sin que pierda sus propiedades mecánicas.
Fue uno de los primeros metales en ser utilizado por el ser humano en la prehistoria. El cobre y su aleación con el estaño, el bronce, adquirieron tanta importancia que los historiadores han llamado Edad del Cobre y Edad del Bronce a dos periodos de la Antigüedad. Aunque su uso perdió importancia relativa con el desarrollo de la siderurgia, el cobre y sus aleaciones siguieron siendo empleados para hacer objetos tan diversos como monedas, campanas y cañones. A partir del siglo XIX, concretamente de la invención del generador eléctrico en 1831 por Faraday, el cobre se convirtió de nuevo en un metal estratégico, al ser la materia prima principal de cables e instalaciones eléctricas.
El cobre posee un importante papel biológico en el proceso de fotosíntesis de las plantas, aunque no forma parte de la composición de la clorofila. El cobre contribuye a la formación de glóbulos rojos y al mantenimiento de los vasos sanguíneos, nervios, sistema inmunológico y huesos y por tanto es un oligoelemento esencial para la vida humana.
El cobre se encuentra en una gran cantidad de alimentos habituales de la dieta tales como ostras, mariscos, legumbres, vísceras y nueces entre otros, además del agua potable y por lo tanto es muy raro que se produzca una deficiencia de cobre en el organismo. El desequilibrio de cobre ocasiona en el organismo una enfermedad hepática conocida como enfermedad de Wilson.[10]
El cobre es el tercer metal más utilizado en el mundo, por detrás del acero y el aluminio. La producción mundial de cobre refinado se estimó en 15,8 Mt en el 2006, con un déficit de 10,7% frente a la demanda mundial proyectada de 17,7 Mt.[11]
Engels Matos Ing. Civil I-003D -
Nombre, símbolo, número: Cloro, Cl, 17
Serie química: Halógenos
Densidad: 3,214 kg/m3
Apariencia: amarillo verdoso
Masa atómica: 35,453 u
Radio medio: 100 pm
Radio atómico calculado: 79 pm
Radio covalente: 99 pm
Radio de Van der Waals: 175 pm
Configuración electrónica: [Ne]3s2 3p5
Estados de oxidación: (Óxido) ±1, +3, +5, +7 (ácido fuerte)
Estructura cristalina: Ortorrómbica
Estado de la materia: gas (no magnético)
Punto de fusión: 171,6 K
Punto de ebullición: 239,11 K
Entalpía de vaporización: 10,2 kJ/mol
Entalpía de fusión: 3,203 kJ/mol
Presión de vapor: 1300 Pa
Velocidad: del sonido sin datos
El cloro (del griego χλωρος, que significa "amarillo verdoso") fue descubierto en su forma diatómica en 1774 por el sueco Carl Wilhelm Scheele, aunque creía que se trataba de un compuesto que contenía oxígeno. Lo obtuvo a partir de la siguiente reacción:
2 NaCl + 2H2SO4 + MnO2 → Na2SO4 + MnSO4 + 2 H2O + Cl2
En 1810 el químico inglés Humphry Davy demuestra que se trata de un elemento químico y le da el nombre de cloro debido a su color. El gas cloro se empleó en la Primera Guerra Mundial, siendo el primer caso de uso de armas químicas.
I Guerra Mundial
El gas cloro, también conocido como bertholita, fue usado como un arma en la I Guerra Mundial por Alemania el 22 de abril de 1915, en la Segunda Batalla de Ypres. Como lo describieron los soldados, tenía un olor distintivo de una mezcla entre pimienta y piña. También tenía gusto metálico y pungía el fondo de la garganta y el pecho. El cloro puede reaccionar con el agua en la mucosa de los pulmones para formar ácido clorhídrico, un irritante que puede ser letal. El daño hecho por el gas de cloro puede ser evitado por una máscara de gas, u otros métodos de filtración, que hacen que la posibilidad total de morir por gas cloro sea mucho menor que por otras armas químicas.
monica portela I003D Ing Civil -
Es un metal abundante en la naturaleza; se considera que es el cuarto metal estructural más abundante en la superficie terrestre y el noveno en la gama de metales industriales. No se encuentra en estado puro sino en forma de óxidos, en la escoria de ciertos minerales de hierro y en las cenizas de animales y plantas. Su utilización se ha generalizado con el desarrollo de la tecnología aeroespacial, donde es capaz de soportar las condiciones extremas de frío y calor que se dan en el espacio y en la industria química, por ser resistente al ataque de muchos ácidos; asimismo, este metal tiene propiedades biocompatibles, dado que los tejidos del organismo toleran su presencia, por lo que es factible la fabricacion de muchas prótesis e implantes de este metal.
Posee propiedades mecánicas parecidas al acero, tanto puro como en las aleaciones que forma, por tanto compite con el acero en muchas aplicaciones técnicas, especialmente con el acero inoxidable.
El titanio fue declarado material estratégico por parte de Estados Unidos durante muchos años. Puede formar aleaciones con otros elementos, tales como hierro, aluminio, vanadio, molibdeno y otros, para producir componentes muy resistentes que son utilizados por la industria aeroespacial, aeronáutica, militar, petroquímica, agroindustrial, automovilística y médica.
El titanio (llamado así por los Titanes, hijos de Urano y Gea en la mitología griega) fue descubierto en Inglaterra por William Gregor, en 1791, cuando estudiaba un metal de color gris-plata que había encontrado. Poco después, en 1795, el químico alemán Martín Kalprotz, descubridor también del uranio, le dio el nombre de titanio.
Este elemento es, en cuanto a su abundancia, el noveno de los que forman la corteza terrestre. Virtualmente, todas las rocas ígneas, y sus sedimentos, así como muchos minerales, principalmente los que contienen hierro y todos los organismos vegetales y animales, contienen titanio.
El mineral más importante del que se extrae titanio es el rutilo (óxido de titanio), muy abundante en las arenas costeras. Por su parte el titanio debe ser sometido previamente a un proceso metalúrgico de refinado, para prevenir su eventual reacción con sustancias gaseosas, tales como el nitrógeno, el oxígeno y el hidrógeno.
Matthew A. Hunter preparó por primera vez titanio metálico puro (con una pureza del 99.9%) calentando tetracloruro de titanio (TiCl4) con sodio a 700-800 °C en un reactor de acero.
El titanio como metal no se usó fuera del laboratorio hasta que en 1946 William Justin Kroll desarrolló un método para poder producirlo comercialmente, mediante la reducción del TiCl4 con magnesio, y este método, llamado Método de Kroll, es el utilizado aún hoy en día (2008). En este proceso el metal se mantiene constantemente en una atmósfera de gas inerte, como argón o helio, que inhibe la reacción con cualquier otro elemento.[1]
Durante los años 50 y 60 la Unión Soviética promovió el empleo de titanio en usos militares y submarinos (Clase Alfa y Clase Miguel) como parte de sus programas militares relacionados con la guerra fría. En los EE. UU., el Departamento de Defensa (DOD) comprendió la importancia estratégica del metal y apoyó los esfuerzos para su comercialización. A lo largo del período de la guerra fría, el gobierno estadounidense consideró al titanio como un material estratégico, y las reservas de esponja de titanio fueron mantenidas por el Centro de Reservas Nacional de Defensa, que desapareció en 2005. Hoy el mayor productor mundial es el consorcio ruso VSMPO-AVISMA, que representa aproximadamente el 29% de la cuota mundial de mercado.
En 2006, la Agencia de Defensa estadounidense concedió 5,7 millones de dólares a un consorcio de dos empresas para desarrollar un nuevo proceso para fabricar polvo de metal de titanio. Bajo calor y presión, se puede usar el polvo para crear artículos fuertes, de peso ligero en las superficies de revestimiento de armaduras o componentes para el espacio aéreo, el transporte e industrias de tratamiento químico.
caracteristicas quimicas: * Se encuentra en forma de óxido, en la escoria de ciertos minerales y en cenizas de animales y plantas.
* Presenta dimorfismo, a temperatura ambiente tiene estructura hexagonal compacta (hcp) llamada fase alfa. Por encima de 882 ºC presenta estructura física centrada en el cuerpo (bcc) se conoce como fase beta.
* La resistencia a la corrosión que presenta es debida al fenómeno de pasivación que sufre (se forma un óxido que lo recubre). Es resistente a temperatura ambiente al ácido sulfúrico (H2SO4) diluido y al ácido clorhídrico (HCl) diluido, así como a otros ácidos orgánicos, también es resistente a las bases, incluso en caliente. Sin embargo se puede disolver en ácidos en caliente. Asimismo, se disuelve bien en ácido fluorhídrico (HF), o con fluoruros en ácidos. A temperaturas elevadas puede reaccionar fácilmente con el nitrógeno, el oxígeno, el hidrógeno, el boro y otros no metales.
* Sus iones no tienen existencia a pH básicos.
darlis giran I003D Ing Civil 2 semestre -
se caracteriza Sus propiedades son intermedias entre las del carbono y el germanio. En forma cristalina es muy duro y poco soluble y presenta un brillo metálico y color grisáceo. Aunque es un elemento relativamente inerte y resiste la acción de la mayoría de los ácidos, reacciona con los halógenos y álcalis diluidos. El silicio transmite más del 95% de las longitudes de onda de la radiación infrarroja.
Se prepara en forma de polvo amorfo amarillo pardo o de cristales negros-grisáceos. Se obtiene calentando sílice, o dióxido de silicio (SiO2), con un agente reductor, como carbono o magnesio, en un horno eléctrico. El silicio cristalino tiene una dureza de 7, suficiente para rayar el vidrio, de dureza de 5 a 7. El silicio tiene un punto de fusión de 1.411 °C, un punto de ebullición de 2.355 °C y una densidad relativa de 2,33. Su masa atómica es 28,086.
Se disuelve en ácido fluorhídrico formando el gas tetrafluoruro de silicio, SiF4 (ver flúor), y es atacado por los ácidos nítrico, clorhídrico y sulfúrico, aunque el dióxido de silicio formado inhibe la reacción. También se disuelve en hidróxido de sodio, formando silicato de sodio y gas hidrógeno. A temperaturas ordinarias el silicio no es atacado por el aire, pero a temperaturas elevadas reacciona con el oxígeno formando una capa de sílice que impide que continúe la reacción. A altas temperaturas reacciona también con nitrógeno y cloro formando nitruro de silicio y cloruro de silicio respectivamente.
El silicio constituye un 28% de la corteza terrestre. No existe en estado libre, sino que se encuentra en forma de dióxido de silicio y de silicatos complejos. Los minerales que contienen silicio constituyen cerca del 40% de todos los minerales comunes, incluyendo más del 90% de los minerales que forman rocas volcánicas. El mineral cuarzo, sus variedades (cornalina, crisoprasa, ónice, pedernal y jaspe) y los minerales cristobalita y tridimita son las formas cristalinas del silicio existentes en la naturaleza. El dióxido de silicio es el componente principal de la arena. Los silicatos (en concreto los de aluminio, calcio y magnesio) son los componentes principales de las arcillas, el suelo y las rocas, en forma de feldespatos, anfíboles, piroxenos, micas y ceolitas, y de piedras semipreciosas como el olivino, granate, zircón, topacio y turmalina.
Silicio como base bioquímica Sus características compartidas con el carbono, como estar en la misma familia 14, no ser metal propiamente dicho, poder construir compuestos parecidos a las enzimas (zeolitas), otros compuestos largos con oxigeno (siliconas) y poseer los mismos cuatro enlaces básicos, le confiere cierta oportunidad en llegar a ser base de seres vivos, aunque no sea en la tierra, en una bioquímica hipotética.
maria alejandra urbina I003D Ing. Civil 2 Semestre -
El magnesio no se encuentra en la naturaleza en estado libre (como metal), sino que forma parte de numerosos compuestos, en su mayoría óxidos y sales. El magnesio elemental es un metal liviano, medianamente fuerte, color blanco plateado. En contacto con el aire se vuelve menos lustroso, aunque a diferencia de otros metales alcalinos no necesita ser almacenado en ambientes libres de oxígeno, ya que está protegido por una fina capa de óxido, la cual es bastante impermeable y difícil de sacar.
Como su vecino inferior de la tabla periódica, el calcio, el magnesio reacciona con agua a temperatura ambiente, aunque mucho más lento. Cuando se sumerge en agua, en la superficie del metal se forman pequeñas burbujas de hidrógeno, pero si es pulverizado reacciona más rápidamente.
El magnesio también reacciona con ácido clorhídrico (HCl) produciendo calor e hidrógeno, que se libera al ambiente en forma de burbujas. A altas temperaturas la reacción ocurre aún más rápido.
En química orgánica es un metal ampliamente empleado al ser necesario para la síntesis de reactivos de Grignard.
El magnesio es un metal altamente inflamable, que entra en combustión fácilmente cuando se encuentra en forma de virutas o polvo, mientras que en forma de masa sólida es menos inflamable. Una vez encendido es difícil de apagar, ya que reacciona tanto con nitrógeno presente en el aire (formando nitrato de magnesio) como con dióxido de carbono (formando óxido de magnesio y carbono). Al arder en aire, el magnesio produce una llama blanca muy intensa incandescente, la cual fue muy utilizada en los comienzos de la fotografía. En ese tiempo se usaba el polvo de magnesio como la fuente de iluminación (polvo de flash). Más tarde, se usarían tiras de magnesio en bulbos de flash eléctricos. El polvo de magnesio todavía se utiliza en la fabricación de fuegos artificiales y en bengalas marítimas.
El magnesio es importante para la vida, tanto animal como vegetal. La clorofila (que interviene en la fotosíntesis) es una sustancia compleja de porfirina-magnesio.
gredys aular petroquimica 005 II sem. -
Nro. atomico 16
simbolo "S" (del latin Sulphur)
Es un no metal abundante e insípido. El azufre se encuentra en forma nativa en regiones volcánicas y en sus formas reducidas formando sulfuros y sulfonales o bien en sus formas oxidadas como sulfatos. Es un elemento químico esencial para todos los organismos y necesario para muchos aminoácidos y, por consiguiente, también para las proteínas. Se usa principalmente como fertilizante pero también en la fabricación de pólvora, laxantes, cerillas e insecticidas.Este no metal tiene un color amarillo, es blando, frágil, ligero, desprende un olor característico a huevo podrido al mezclarse con hidrógeno y arde con llama de color azul, desprendiendo dióxido de azufre. Es insoluble en agua pero se disuelve en disulfuro de carbono.
El azufre es un elemento muy abundante en la corteza terrestre, se encuentra en grandes cantidades combinado en forma de sulfuros (pirita, galena) y de sulfatos (aljez). En forma nativa se encuentra en las cercanías de aguas termales, zonas volcánicas y en minas de cinabrio, galena, esfalerita y estibina, y en Luisiana (Estados Unidos, primer productor mundial) se extrae mediante el proceso Frasch consistente en inyectar vapor de agua sobrecalentado para fundir el azufre que posteriormente es bombeado al exterior utilizando aire comprimido.También se obtiene separándolo de gas natural, si bien su obtención anteriormente era a partir de depósitos de azufre puro impregnado en cenizas volcánicas (Italia, y más recientemente Argentina).
"En el Génesis (19,24), los hebreos decían que Dios (Yahvé) hizo llover sobre Sodoma y sobre Gomorra sulfuro y fuego desde el cielo.
Homero recomendaba, en el siglo IX aec, evitar la pestilencia del azufre (zeio en griego, relacionado con zeos-Zeus)."
Luis Arvelo CI.22.414.117 Ing. Petroquímica i-005 2do Semestre -
El sodio ocupa el sexto lugar por su abundancia entre todos los elementos de la corteza terrestre, que contiene el 2.83% de sodio en sus formas combinadas. El sodio es, después del cloro, el segundo elemento más abundante en solución en el agua de mar. Las sales de sodio más importantes que se encuentran en la naturaleza son el cloruro de sodio (sal de roca), el carbonato de sodio (sosa y trona), el borato de sodio (bórax), el nitrato de sodio (nitrato de Chile) y el sulfato de sodio. Las sales de sodio se encuentran en el agua de mar, lagos salados, lagos alcalinos y manantiales minerales.
El sodio reacciona con rapidez con el agua, y también con nieve y hielo, para producir hidróxido de sodio e hidrógeno. Cuando se expone al aire, el sodio metálico recién cortado pierde su apariencia plateada y adquiere color gris opaco por la formación de un recubrimiento de óxido de sodio. El sodio no reacciona con nitrógeno, incluso a temperaturas muy elevadas, pero puede reaccionar con amoniaco para formar amida de sodio. El sodio y el hidrógeno reaccionan arriba de los 200ºC (390ºF) para formar el hidruro de sodio. El sodio reacciona difícilmente con el carbono, si es que reacciona, pero sí lo hace con los halógenos. También reacciona con varios halogenuros metálicos para dar el metal y cloruro de sodio.
El sodio no reacciona con los hidrocarburos parafínicos, pero forma compuesto de adición con naftaleno y otros compuestos aromáticos policíclicos y con aril alquenos. La reacción del sodio con alcoholes es semejante a la reacción del sodio con agua, pero menos rápida. Hay dos reacciones generales con halogenuros orgánicos. Una de éstas requiere la condensación de dos compuesto orgánicos que contengan halógenos al eliminar éstos. El segundo tipo de reacciones incluye el reemplazo del halógeno por sodio, para obtener un compuesto organosódico.
Y su distribucion electronica es:
Na=11
11e= 1s2 2s2 2p6 3s1
Nataly Buinitzky CI. 21.327.393 Ing. Petroquimica I-005 2do Semestre -
El zinc es un metal de color blanco azulado, que actúa como divalente, teniendo en su último nivel la estructura ns2, siendo n=4, y en el penúltimo nivel contiene 18 electrones. El zinc (Zn), junto con el cadmio y el mercurio, constituye el grupo IIB de la tabla periódica con la siguiente estructura o distribución elecrónica:
Zinc (Zn)=30
30e= 1s2 2s2 2p6 3s2 3p6 3d10 4s2
No existen isotopos radiactivos naturales del zinc. El peso atómico es de 65.30 y la distribución de sus isotopos es:
64-48.9%; 66-27.8%; 68-18.6%; 67-4.0%; 70-0.7%
Es bastante quebradizo a la temperatura ordinaria, pero calentado entre 100 y 150°C es blando y manejable, de manera que puede ser laminado y estirado en hilos por medio de rodillos calientes, manteniendo después su flexibilidad al enfriarse. De 200° a 300°C se vuelve de nuevo quebradizo.
Este metal se disuelve con la mayoría de los ácidos minerales, pero el zinc de alta pureza, resiste el ataque del ácido sulfúrico deluido debido a la sobretensión de Hidrógeno.
En forma granulada o pulverulenta el zinc es ampliamente utilizado como precipitante, siendo reductor de iones tales como los ferricos, manganatos, y cromatos.
teorileth chavez ing.petroquimica 005 -
configuracion electronica
Z = 1 Hidrógeno
H: 1s1
El hidrógeno es un elemento químico representado por el símbolo H y con un número atómico de 1. En condiciones normales de presión y temperatura, es un gas diatómico (H2) incoloro, inodoro, insípido, no metálico y altamente inflamable. Con una masa atómica de 1,00794(7) u, el hidrógeno es el elemento químico más ligero y es, también, el elemento más abundante, constituyendo aproximadamente el 75% de la materia visible del universo.[1]
En su ciclo principal, las estrellas están compuestas por hidrógeno en estado de plasma. El hidrógeno elemental es muy escaso en la Tierra y es producido industrialmente a partir de hidrocarburos como, por ejemplo, el metano. La mayor parte del hidrógeno elemental se obtiene "in situ", es decir, en el lugar y en el momento en el que se necesita. El hidrógeno puede obtenerse a partir del agua por un proceso de electrólisis, pero resulta un método mucho más caro que la obtención a partir del gas natural.
Sus principales aplicaciones industriales son el refinado de combustibles fósiles (por ejemplo, el hidrocracking) y la producción de amoníaco (usado principalmente para fertilizantes).
El isótopo del hidrógeno más común en la naturaleza, conocido como protio (término muy poco usado), tiene un solo protón y ningún neutrón. En los compuestos iónicos, el hidrógeno puede adquirir carga positiva (convirtiéndose en un catión compuesto únicamente por el protón) o negativa (convirtiéndose en un anión conocido como hidruro).
El hidrógeno puede formar compuestos con la mayoría de los elementos y está presente en el agua y en la mayoría de los compuestos orgánicos. Desempeña un papel particularmente importante en la química ácido - base, en la que muchas reacciones conllevan el intercambio de protones entre moléculas solubles. Puesto que es el único átomo neutro para el cual la ecuación de Schrödinger puede ser resuelta analíticamente, el estudio de la energía y del enlace del átomo de hidrógeno ha sido fundamental para el desarrollo de la mecánica cuántica.
maria perdomo ing.petroqumica 005 20.445.212 -
Es un metal maleable, de color gris plateado y presenta propiedades magn¨¦ticas; es ferromagn¨¦tico a temperatura ambiente y presi¨®n atmosf¨¦rica.
Se encuentra en la naturaleza formando parte de numerosos minerales, entre ellos muchos ¨®xidos, y raramente se encuentra libre. Para obtener hierro en estado elemental, los ¨®xidos se reducen con carbono y luego es sometido a un proceso de refinado para eliminar las impurezas presentes.
Es el elemento m¨¢s pesado que se produce exot¨¦rmicamente por fusi¨®n, y el m¨¢s ligero que se produce a trav¨¦s de una fisi¨®n, debido a que su n¨²cleo tiene la m¨¢s alta energ¨ªa de enlace por nucle¨®n (energ¨ªa necesaria para separar del n¨²cleo un neutr¨®n o un prot¨®n); por lo tanto, el n¨²cleo m¨¢s estable es el del hierro-56 (con 30 neutrones).
Presenta diferentes formas estructurales dependiendo de la temperatura y presi¨®n. A presi¨®n atmosf¨¦rica:
Hierro-¦Á: estable hasta los 911 ¡ãC. El sistema cristalino es una red c¨²bica centrada en el cuerpo (bcc).
Hierro-¦Ã: 911 ¡ãC - 1392 ¡ãC; presenta una red c¨²bica centrada en las caras (fcc).
Hierro-¦Ä: 1392 ¡ãC - 1539 ¡ãC; vuelve a presentar una red c¨²bica centrada en el cuerpo.
Hierro-¦Å: Puede estabilizarse a altas presiones, presenta estructura hexagonal compacta (hcp).
El hierro-¦Á es ferromagn¨¦tico hasta la temperatura de Curie (768 ¡ãC), a partir de la cual pasa a ser paramagn¨¦tico. Antiguamente, al hierro-¦Á paramagn¨¦tico se le llamaba hierro-¦Â, aunque hoy en d¨ªa no se suele distinguir entre las fases ¦Á y ¦Â.
configuracion electronica
Z:26 Fe: 1s22s22p63s23p63d64s2
Jesiree diaz ING:petroquimica 005 20.194.534 -
Elemento químico, Ca, de número atómico 20; es el quinto elemento y el tercer metal más abundante en la corteza terrestre. Los compuestos de calcio constituyen 3.64% de la corteza terrestre. El metal es trimorfo, más duro que el sodio, pero más blando que el aluminio. Al igual que el berilio y el aluminio, pero a diferencia de los metales alcalinos, no causa quemaduras sobre la piel. Es menos reactivo químicamente que los metales alcalinos y que los otros metales alcalinotérreos. La distribución del calcio es muy amplia; se encuentra en casi todas las áreas terrestres del mundo. Este elemento es esencial para la vida de las plantas y animales, ya que está presente en el esqueleto de los animales, en los dientes, en la cáscara de los huevos, en el coral y en muchos suelos. El cloruro de calcio se halla en el agua del mar en un 0.15%.
Los iones calcio disueltos en el agua forman depósitos en tuberías y calderas cuando el agua es dura, es decir, cuando contiene demasiado calcio o magnesio. Esto se puede evitar con los ablandadores de agua.
El calcio metálico se prepara en la industria por electrólisis del cloruro de calcio fundido. Éste se obtiene por tratamiento de los minerales de carbonato con ácido clorhídrico o como un desperdicio del proceso Solvay de los carbonatos. El metal puro puede ser maquinado en torno, hilado, serrado, extruido; se le puede convertir en alambre, prensar y amartillar en placas.
El calcio forma una película fina de óxido y nitruro en el aire, la cual lo protege de un ataque posterior. Se quema en el aire a temperatura elevada para producir principalmente nitruro.
El metal producido en forma comercial reacciona fácilmente con el agua y los ácidos y produce hidrógeno que contiene cantidades notables de amoniaco e hidrocarburos como impurezas.
El metal se emplea en aleaciones de aluminio para cojinetes, como auxiliar en la remoción del bismuto del plomo, así como controlador de carbono grafítico en el hierro fundido. Se emplea también como desoxidante en la manufactura de muchos aceros; como agente reductor en la preparación de metales como el cromo, torio, zirconio y uranio, y como material de separación para mezclas gaseosas de nitrógeno y argón.
El óxido de calcio, CaO, se produce por descomposición térmica de los minerales de carbonato en altos hornos, aplicando un proceso de lecho continuo. El óxido se utiliza en arcos de luz de alta intensidad (luz de cal) a causa de sus características espectrales poco usuales y como agente deshidratante industrial. La industria metalúrgica hace amplio uso del óxido durante la reducción de aleaciones ferrosas.
El hidróxido de calcio, Ca(OH)2, tiene muchas aplicaciones en donde el ión hidroxilo es necesario. En el proceso de apagado del hidróxido de calcio, el volumen de cal apagada [Ca(OH)2] se expande al doble que la cantidad de cal viva inicial (CaO), hecho que lo hace útil para romper roca o madera.
La cal apagada es un absorbente excelente para el dióxido de carbono, al producir el carbonato que es muy insoluble.
El siliciuro de calcio, CaSi, preparado en horno eléctrico a partir de cal, sílice y agentes reductores carbonosos, es útil como agente desoxidante del acero. El carburo de calcio, CaC2, se produce al calentar una mezcla de cal y carbón a 3000ºC (5432ºF) en un horno eléctrico y es un acetiluro que produce acetileno por hidrólisis. El acetileno es el material base de un gran número de productos químicos importantes en la química orgánica industrial.
El carbonato de calcio puro existe en dos formas cristalinas: la calcita, de forma hexagonal, la cual posee propiedades de birrefrigencia, y la aragonita, de forma romboédrica. Los carbonatos naturales son los minerales de calcio más abundantes. El espato de Islandia y la calcita son formas esencialmente puras de carbonato, mientras que el mármol es impuro y mucho más compacto, por lo que puede pulirse. Tiene gran demanda como material de construcción. Aunque el carbonato de calcio es muy poco soluble en agua, tiene una solubilidad considerable en agua que contenga dióxido de carbono disuelto, ya que en estas soluciones forma el bicarbonato al disolverse. Este hecho explica la formación de cavernas, donde los depósitos de piedra caliza han estado en contacto con aguas ácidas.
Los halogenuros de calcio incluyen el fluoruro fosforescente, que es el compuesto de calcio más abundante y con aplicaciones importantes en espectroscopia. El cloruro de calcio posee, en la forma anhidra, capacidad notoria de delicuescencia que lo hace útil como agente deshidratante industrial y como factor de control de tolvaneras en carreteras. El hipoclorito de calcio (polvo blanqueador) se produce en la industria al pasar cloro dentro de una solución de cal, y se ha utilizado como agente blanqueador y purificador de agua.
El sulfato de calcio dihidratado es el yeso mineral, constituye la mayor porción del cemento Portland, y se ha empleado para reducir la alcalinidad de los suelos. Un hemihidrato del sulfato de calcio se produce por calentamiento del yeso a temperaturas altas, y se vende con el nombre comercial de estuco de París.
El calcio es un constituyente invariable de todas las plantas, ya que es esencial para su crecimiento. Lo contienen como constituyente estructural y como ion fisiológico. El calcio se encuentra en el tejido blando, en fluidos tisulares y en la estructura del esqueleto de todos los animales. Los huesos de los vertebrados contienen calcio en forma de fluoruro de calcio, carbonato de calcio y fosfato de calcio.
Distribucion electronica
La notación espectral del Calcio (Z = 20) es: 1s2 2s2 2p6 3s2 3p6 4s2
Katherine Alvarado. CI: 20.296.369. ING Petroquimíca. Sección:I005D -
El potasio es un elemento químico de la tabla periódica cuyo símbolo es K (del latín Kalium) y cuyo numero atómico es 19 y peso atómico 39.098. Ocupa un lugar intermedio dentro de la familia de los metales alcalinos después del sodio y antes del rubidio. Este metal reactivo es ligero y blando.
Es un metal alcalino, blanco-plateado que abunda en la naturaleza, Se oxida rápidamente en el aire, es muy reactivo, especialmente en agua. El potasio constituye del orden del 2,4% en peso de la corteza terrestre siendo el séptimo más abundante. Debido a su solubilidad es muy difícil obtener el metal puro a partir de sus minerales.En el año 1807, el Sir Humphrey Davy descubrió el potasio en Gran Bretaña. En 1.807 Davy aisló por primera vez el metal por electrólisis del hidróxido potásico húmedo.
El potasio puede ser encontrado en vegetales, frutas, patatas, carne, pan, leche y frutos secos. Juega un importante papel en los sistemas de fluidos físicos de los humanos y asiste en las funciones de los nervios. Cuando nuestros riñones no funcionan bien se puede dar la acumulación de potasio. Esto puede llevar a cabo una perturbación en el ritmo cardiáco.
En cuanto a las propiedades fisicas del potacio:
Valencia 1, Estado de oxidación +1, Electronegatividad 0,8 , Radio covalente (Å) 1,96, Radio iónico (Å) 1,33, Radio atómico (Å) 2,35, Configuración electrónica [Ar]4s1, Primer potencial de ionización (eV) 4,37, Masa atómica (g/mol) 39,098, Densidad (g/ml) 0,97, Punto de ebullición (ºC) 760, Punto de fusión (ºC) 97,8, Distribucion electrónica del potasio es 1s2 2s2 2p6 3s2 3p6 4s1.
El potasio metal se usa en células fotoeléctricas.
El cloruro y el nitrato se emplean como fertilizantes.
El peróxido de potasio se usa en aparatos de respiración autónomos de bomberos y mineros.
El nitrato se usa en la fabricación de pólvora y el cromato y dicromato en pirotecnia.
El carbonato potásico se emplea en la fabricación de cristales.
La aleación NaK, es un material empleado para la transferencia de calor.
El cloruro de potasio se utiliza para provocar un paro cardíaco en las ejecuciones con inyección letal.